 Ils disent que la vie est un processus continu de vieillissement qui se termine inévitablement par la mort. Cela peut ne pas sembler très optimiste, mais telles sont les lois de la nature. Le vieillissement et la mort sont parmi les régulateurs les plus importants d'une population de toute nature sur la planète, et l'immortalité au sens biologique du terme n'existe que dans les livres et les films. La même situation est avec la jeunesse "éternelle". Dans les livres, nous avons Dorian Gray - un jeune homme éternellement jeune et beau avec une forte antipathie pour une œuvre d'art particulière; Edward Cullen est un vampire éternellement jeune avec une carence en vitamine D et une réflectivité cutanée élevée, etc. En réalité, la jeunesse éternelle ou du moins prolongée est inaccessible. Du moins si les scientifiques n'interfèrent pas dans le processus. Aujourd'hui, nous apprendrons l'étude,dans lequel des scientifiques de l'Université de Stanford ont réussi à rajeunir les vieilles cellules humaines grâce à certaines protéines impliquées dans le processus de développement embryonnaire. Quelles substances ont été utilisées, quel âge les cellules étaient-elles plus jeunes et quelle a été la durée de l'effet? Nous en apprenons sur le rapport du groupe de recherche. Aller.
Ils disent que la vie est un processus continu de vieillissement qui se termine inévitablement par la mort. Cela peut ne pas sembler très optimiste, mais telles sont les lois de la nature. Le vieillissement et la mort sont parmi les régulateurs les plus importants d'une population de toute nature sur la planète, et l'immortalité au sens biologique du terme n'existe que dans les livres et les films. La même situation est avec la jeunesse "éternelle". Dans les livres, nous avons Dorian Gray - un jeune homme éternellement jeune et beau avec une forte antipathie pour une œuvre d'art particulière; Edward Cullen est un vampire éternellement jeune avec une carence en vitamine D et une réflectivité cutanée élevée, etc. En réalité, la jeunesse éternelle ou du moins prolongée est inaccessible. Du moins si les scientifiques n'interfèrent pas dans le processus. Aujourd'hui, nous apprendrons l'étude,dans lequel des scientifiques de l'Université de Stanford ont réussi à rajeunir les vieilles cellules humaines grâce à certaines protéines impliquées dans le processus de développement embryonnaire. Quelles substances ont été utilisées, quel âge les cellules étaient-elles plus jeunes et quelle a été la durée de l'effet? Nous en apprenons sur le rapport du groupe de recherche. Aller.Base d'étude
Qu'est-ce que le vieillissement? À la base, il s'agit d'un processus de perte progressive de fonctionnalité au niveau des molécules, des cellules, des tissus et de l'organisme tout entier.Au niveau de la chromatine * , le vieillissement est associé à une accumulation progressive d' erreurs épigénétiques * , qui conduisent finalement à une régulation génique aberrante (anormale), à une déplétion des cellules souches, au vieillissement et à une homéostasie cellulaire / tissulaire altérée.Chromatine * - la base des chromosomes, composée d'ADN et de protéines (principalement des histones). La chromatine est située à l'intérieur du noyau des cellules eucaryotes (organismes qui ont un noyau dans les cellules) et fait partie du nucléoïde des procaryotes (unicellulaire sans noyau).
Hérédité épigénétique * - ensemble de modifications héréditaires du phénotype ou de l'expression des gènes.
Si vous appliquez une reprogrammation nucléaire des cellules pluripotence * , vous pouvez inverser son âge, mais pas son identité.La pluripotence * est une caractéristique d'une cellule qui peut se différencier en tous les types de cellules, à l'exception des cellules des organes extra-germinaux.
Auparavant, cette technique avait déjà été testée sur des souris. Les résultats ont été très encourageants, car la reprogrammation temporaire a amélioré les caractéristiques d'âge et prolongé la durée de vie des souris. Mais l'homme n'est pas une souris, et la question reste donc de savoir comment cette technique fonctionnera sur les cellules humaines. C'est exactement ce que les scientifiques envisagent dans cette étude.Le processus de reprogrammation nucléaire en cellules souches pluripotentes induites ( iPSC * ) est caractérisé par une réinitialisation complète (réinitialisation) des caractéristiques épigénétiques des cellules, ce qui conduit au retour de l'identité cellulaire et de l'âge à un état embryonnaire.Les cellules souches pluripotentes induites (iPSC) * sont un type de cellules souches obtenues en laboratoire à partir de cellules différenciées matures d'un organisme mammifère (y compris l'homme).
Il est curieux que la reprogrammation ne soit pas irréversible, s'arrêtant au soi-disant point de non-retour (PNR à partir du point de non-retour), après quoi les cellules retrouvent finalement leur état somatique * d' origine .Cellule somatique * - cellules qui composent le soma (corps du corps), mais non impliquées dans le développement sexuel.
Par conséquent, si la reprogrammation affecte la cellule pendant une période de temps assez courte, alors l'expression des facteurs de reprogrammation ne pourra pas effacer la signature épigénétique qui détermine l'identité des cellules. Il s'avère qu'une courte exposition ne changera pas l'identité de la cellule, mais peut-elle affecter son âge?La première preuve que la reprogrammation temporaire peut améliorer les phénotypes au cours du vieillissement a été montrée chez la souris. Mais, comme les scientifiques nous l'ont déjà rappelé, les souris ne sont pas des humains. Une question importante de cette technique est de savoir si elle peut fonctionner sur des cellules humaines naturelles isolées de personnes âgées.Pour le savoir, les scientifiques ont mené une série d'expériences pour identifier le degré d'impact de la reprogrammation nucléaire sur les phénotypes (signes externes et internes) des cellules humaines et murines.Résultats de recherche
Tout d'abord, une évaluation a été faite de l'effet de l'expression transitoire des facteurs de reprogrammation sur la transcription de deux types différents de cellules ( fibroblastes * et cellules endothéliales * ) chez les personnes âgées. Ensuite, la transcription des personnes âgées a été comparée avec la transcription des mêmes types cellulaires de jeunes donneurs ( 1a et 1e ).Fibroblaste * - cellules du tissu conjonctif du corps qui synthétisent la matrice extracellulaire.
Endothélium * - une couche de cellules plates sur les parois internes des vaisseaux sanguins, des vaisseaux lymphatiques et des cavités cardiaques.
 Image n ° 1Les fibroblastes ont été obtenus à partir d' échantillons de biopsie * de la peau des mains et de l'abdomen des participants à l'étude: 3 personnes âgées de 25 à 35 ans (groupe jeune) et 8 personnes âgées de 60 à 90 ans (groupe âgé).
Image n ° 1Les fibroblastes ont été obtenus à partir d' échantillons de biopsie * de la peau des mains et de l'abdomen des participants à l'étude: 3 personnes âgées de 25 à 35 ans (groupe jeune) et 8 personnes âgées de 60 à 90 ans (groupe âgé).Biopsie * - matériel biologique obtenu par biopsie.
Les cellules endothéliales ont été extraites de la veine et de l'artère iliaques des participants à l'étude: 3 personnes âgées de 15 à 25 ans (groupe jeune) et 8 personnes âgées de 50 à 65 ans (groupe âgé).Pour les expériences, un protocole de reprogrammation non intégrative a été utilisé, qui a été optimisé sur la base d'un ensemble d'ARNm exprimant les protéines OCT4, SOX2, KLF4, c-MYC, LIN28 et NANOG.Ce protocole produit séquentiellement des colonies iPSC, quel que soit l'âge des donneurs, après 12 à 15 transfections quotidiennes * .La transfection * est le processus d'introduction d'acide nucléique dans les cellules eucaryotes par la méthode non virale.
Il a été constaté que le point de non retour dans ce cas est observé le cinquième jour de reprogrammation. Cette conclusion est basée sur le fait que la première expression détectable d' ARNc associé à la pluripotence endogène se produit au jour 58.les ARNdn (ARN longs non codants) * sont des molécules d'ARN situées dans le noyau ou dans le cytoplasme qui ne sont pas traduites en protéines.
Compte tenu de cela, il a été décidé d'utiliser un régime temporaire d'expression exogène dans lequel OSKMLN a été transfecté quotidiennement pendant 4 jours consécutifs, et l'analyse de l'expression des gènes a été effectuée 2 jours après l'interruption ( 1b ).Ensuite, le séquençage de l'ARN de masse apparié a été effectué pour les deux types de cellules dans les trois groupes de sujets: jeunes (Y), personnes âgées sans reprogrammation (UA) et personnes âgées avec reprogrammation (TA).Pour commencer, les scientifiques ont comparé les transcriptions normalisées quantiles de jeunes sujets et de personnes âgées sans reprogrammation (Y et UA). L'analyse a montré que 961 gènes (5,85%) dans les fibroblastes ( 1a et 1c ) et 748 gènes (4,80%) dans les cellules endothéliales ( 1e et 1f) différait entre les cellules jeunes et vieilles.Ces ensembles de gènes sont directement liés aux processus de vieillissement. La détermination de la direction d'expression au-dessus ou au-dessous de la valeur moyenne de chaque gène a montré une nette similitude entre les cellules des jeunes et les cellules des personnes âgées après reprogrammation pour les fibroblastes et les cellules endothéliales ( 1d et 1g ).En utilisant la méthode décrite ci-dessus, les scientifiques ont comparé les populations cellulaires de sujets âgés avec et sans reprogrammation (TA et UA; 1a et 1e ). Il a été constaté que 1042 gènes dans les fibroblastes et 992 dans les cellules endothéliales étaient exprimés de manière différentielle.Ces profils de transcriptome ont ensuite été utilisés pour confirmer la préservation de l'identité cellulaire après reprogrammation. L'analyse a montré qu'il n'y avait pas de changement d'identité significatif.En général, l'analyse des signatures de transcriptome a montré que l'expression OSKLMN favorise une activation très rapide d'un profil d'expression génique plus jeune sans affecter l'expression génique de l'identité cellulaire.Les chercheurs notent que les horloges épigénétiques * basées sur les niveaux de méthylation de l'ADN * sont les biomarqueurs moléculaires les plus précis de l'âge dans les tissus et les cellules. Ils sont également prédictifs de nombreuses conditions liées à l'âge, y compris l'espérance de vie.* — , , .
* — .
Il est également connu que l'expression exogène des facteurs de reprogrammation canoniques (OSKM) ramène l'âge épigénétique des cellules primaires à l'état prénatal.Pour tester si l'expression transitoire OSKMLN peut inverser les horloges épigénétiques des cellules somatiques humaines, les scientifiques ont utilisé deux types d'horloges épigénétiques qui s'appliquent aux fibroblastes et cellules endothéliales humaines: l'horloge épigénétique originale de Panvis Horvath (basée sur 353 paires de cytosine-phosphate-guanine) et plus tard des montres «peau-sang» (basées sur 391 CpG - sites de molécules d'ADN).Calculateur d'âge épigénétique HowarthSelon l'horloge épigénétique de Howart, l'exposition temporaire à OSKMLN a significativement inversé l'âge de la méthylation de l'ADN (différence d'âge moyenne = -3,40 ans). L'effet du rajeunissement était plus prononcé dans les cellules endothéliales (différence d'âge moyenne = -4,94 ans; 1i ) que dans les fibroblastes (différence d'âge moyenne = -1,84; 1 h ).Des résultats qualitativement similaires mais moins significatifs ont été obtenus en utilisant une horloge peau-sang: l'effet global du rajeunissement est de -1,35 ans; le rajeunissement moyen dans les cellules endothéliales est de -1,62 et dans les fibroblastes -1,07.Sur la base de ces résultats, une analyse a été faite de l'effet de la reprogrammation temporaire sur divers signes du vieillissement physiologique cellulaire. Pour cela, une visualisation des cellules individuelles et une vaste base de données des signes de vieillissement ont été réalisées.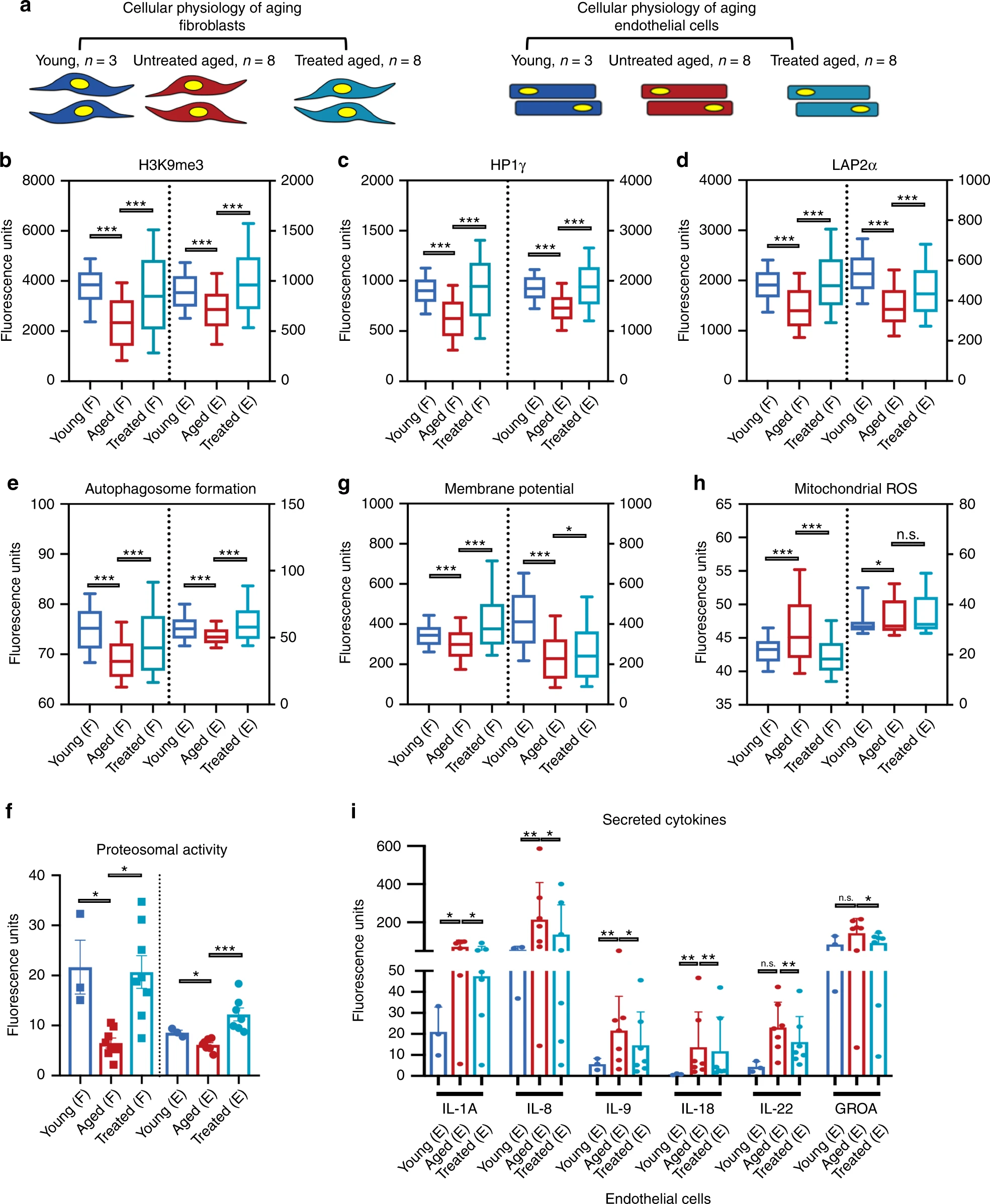 Image n ° 2Toutes les analyses ont été effectuées séparément dans chaque lignée cellulaire distincte ( 2a ): 19 lignées de fibroblastes (3 - jeunes, 8 - âgées et 8 - âgées après reprogrammation) et 17 lignées de cellules endothéliales (3 - jeunes, 7 - âgées et 7 - personnes âgées après reprogrammation). L'analyse statistique a été réalisée par échantillonnage aléatoire de 100 cellules par échantillon.Pour étendre les résultats antérieurs sur l'épigénétique, des mesures quantitatives supplémentaires ont été effectuées en utilisant l'immunofluorescence (IF) du marqueur répressif épigénétique H3K9me3, la protéine HP1γ associée à l'hétérochromatine et la protéine LAP2α supportant la laminine nucléaire * ( 2b - 2d ).
Image n ° 2Toutes les analyses ont été effectuées séparément dans chaque lignée cellulaire distincte ( 2a ): 19 lignées de fibroblastes (3 - jeunes, 8 - âgées et 8 - âgées après reprogrammation) et 17 lignées de cellules endothéliales (3 - jeunes, 7 - âgées et 7 - personnes âgées après reprogrammation). L'analyse statistique a été réalisée par échantillonnage aléatoire de 100 cellules par échantillon.Pour étendre les résultats antérieurs sur l'épigénétique, des mesures quantitatives supplémentaires ont été effectuées en utilisant l'immunofluorescence (IF) du marqueur répressif épigénétique H3K9me3, la protéine HP1γ associée à l'hétérochromatine et la protéine LAP2α supportant la laminine nucléaire * ( 2b - 2d ).Nuclear Lamin * - un réseau rigide fibrillaire sous la membrane nucléaire, qui est impliqué dans l'organisation de la chromatine.
Comme indiqué précédemment dans des études précédentes, dans les fibroblastes matures et les cellules endothéliales, une diminution du signal nucléaire a été observée pour les trois marqueurs par rapport aux cellules jeunes. La reprogrammation des cellules plus anciennes a entraîné une augmentation de ces marqueurs dans les deux types de cellules.Ensuite, l'activité protéolytique (hydrolyse des protéines) des cellules a été étudiée en mesurant la formation d'autophagosomes, et l'activité de protéasome de type chimiotrypsine a également été étudiée. La reprogrammation a non seulement augmenté les deux types d'activité au niveau des jeunes cellules, mais l'a également dépassée ( 2e et 2f ). Cela suggère que les premiers stades de la reprogrammation contribuent à la clairance active des biomolécules dégradées.L'un des signes les plus indicatifs du vieillissement cellulaire est une diminution de l'activité mitochondriale, l'accumulation d'espèces réactives de l'oxygène (ROS) et une dérégulation de la sensibilité aux nutriments. Par conséquent, il est possible de vérifier l'effet de la reprogrammation sur les cellules vieillissantes en mesurant le potentiel membranaire des mitochondries, des mitochondries ROS et des niveaux de protéines de Sirtuin1 (SIRT1).La reprogrammation temporaire a augmenté le potentiel de la membrane mitochondriale dans les deux types de cellules ( 2g ), diminué le ROS mitochondrial ( 2h ) et augmenté les niveaux de protéine SIRT1 dans les fibroblastes, ce qui est observé dans les jeunes cellules.L'imagerie cellulaire par coloration de la bêta-galactosidase associée au vieillissement a montré une diminution significative du nombre de cellules vieillissantes dans les cellules endothéliales, mais pas dans les fibroblastes. Cela s'est accompagné d'une diminution de la quantité de cytokines phénotypiques sécrétoires associées au vieillissement pro-inflammatoire, et à nouveau dans les cellules endothéliales, mais pas dans les fibroblastes ( 2i ).Il a également été constaté que dans aucun des types de cellules la longueur des télomères * ne présente d'allongement significatif après reprogrammation. Cela peut indiquer que les cellules ne se différencient pas dans un état similaire aux cellules souches lorsque l' activité de la télomérase * est réactivée.* — .
* — , 3'- .
Il a également été constaté que les effets de la reprogrammation dans les cellules persistaient même après 4 et 6 jours après l'arrêt de ce processus. Du point de vue de la vitesse de manifestation des effets de reprogrammation, ils ont été observés déjà 2 jours après le début de ce processus.Au total, ces données suggèrent que l'expression transitoire de OSKMLN peut provoquer une amélioration rapide et continue et un changement de l'âge cellulaire dans les cellules somatiques humaines aux niveaux du transcriptome, épigénétique et cellulaire. De plus, ce rajeunissement se produit aux premiers stades de la reprogrammation, raison pour laquelle cette technique n'a pas le temps d'affecter l'identité des cellules.Les scientifiques ont alors décidé de découvrir si l'expression transitoire de l'OSKMNL pouvait également inverser les phénotypes inflammatoires associés au vieillissement. Après avoir obtenu des preuves préliminaires de ce changement dans les cellules endothéliales ( 2j ), l'analyse a été élargie en ajoutant de l'arthrose, une maladie fortement associée au vieillissement et caractérisée par un processus inflammatoire prononcé affectant les chondrocytes dans les articulations.Des échantillons ont été prélevés - des chondrocytes du cartilage de six patients âgés de 60 à 70 ans qui ont subi une opération de remplacement articulaire complète en raison d'une arthrose tardive. De plus, ces échantillons ont subi une reprogrammation et les résultats ont été comparés aux données des chondrocytes de trois jeunes ( 3a ). Image n ° 3L'expression temporaire de l'OSKMLN a été réalisée pendant 2 ou 3 jours, et l'analyse a été réalisée 2 jours après l'interruption de la reprogrammation, bien que les patients aient eu un effet plus durable avec un traitement plus long.Cependant, l'utilisation d'OSKMLN a montré une diminution significative des niveaux d'ARNm intracellulaire de RANKL (cytokine de la famille des facteurs de nécrose tumorale) et d'iNOS2, ainsi que des niveaux de facteurs inflammatoires sécrétés par les cellules ( 3b - 3d ).De plus, une augmentation de la prolifération cellulaire ( 3e ), une augmentation de la production d'ATP ( 3f ) et une diminution du processus oxydatif ( 3g et 3h ) ont été observées .La vérification de l'identité cellulaire a montré que le processus de reprogrammation ne la violait pas: il n'y avait aucun effet sur le niveau d'expression de SOX9, et le niveau d'expression de COL2A1 augmentait significativement (qRT-PCR sur 3i et 3j ).Des résultats ci-dessus, il s'ensuit que l'expression transitoire de OSKMLN peut contribuer à une inversion partielle de l'expression des gènes et de la physiologie cellulaire dans les chondrocytes plus âgés atteints d'arthrose à un état plus jeune. Par conséquent, la technique étudiée peut également être utilisée comme l'une des méthodes de traitement de l'arthrose chez les personnes âgées.Un autre signe important du vieillissement est la perte de la fonction des cellules souches et la perte de la capacité de régénération. Pour tester l'effet de la reprogrammation sur ces facteurs, les scientifiques ont utilisé des cellules souches musculaires squelettiques de souris (MuSC).Les muSC ont été exposés à une reprogrammation pendant 2 jours alors qu'ils étaient au repos. Des individus âgés de 3 mois et 20-24 mois ( 4a ) ont servi de donneurs d'échantillons .
Image n ° 3L'expression temporaire de l'OSKMLN a été réalisée pendant 2 ou 3 jours, et l'analyse a été réalisée 2 jours après l'interruption de la reprogrammation, bien que les patients aient eu un effet plus durable avec un traitement plus long.Cependant, l'utilisation d'OSKMLN a montré une diminution significative des niveaux d'ARNm intracellulaire de RANKL (cytokine de la famille des facteurs de nécrose tumorale) et d'iNOS2, ainsi que des niveaux de facteurs inflammatoires sécrétés par les cellules ( 3b - 3d ).De plus, une augmentation de la prolifération cellulaire ( 3e ), une augmentation de la production d'ATP ( 3f ) et une diminution du processus oxydatif ( 3g et 3h ) ont été observées .La vérification de l'identité cellulaire a montré que le processus de reprogrammation ne la violait pas: il n'y avait aucun effet sur le niveau d'expression de SOX9, et le niveau d'expression de COL2A1 augmentait significativement (qRT-PCR sur 3i et 3j ).Des résultats ci-dessus, il s'ensuit que l'expression transitoire de OSKMLN peut contribuer à une inversion partielle de l'expression des gènes et de la physiologie cellulaire dans les chondrocytes plus âgés atteints d'arthrose à un état plus jeune. Par conséquent, la technique étudiée peut également être utilisée comme l'une des méthodes de traitement de l'arthrose chez les personnes âgées.Un autre signe important du vieillissement est la perte de la fonction des cellules souches et la perte de la capacité de régénération. Pour tester l'effet de la reprogrammation sur ces facteurs, les scientifiques ont utilisé des cellules souches musculaires squelettiques de souris (MuSC).Les muSC ont été exposés à une reprogrammation pendant 2 jours alors qu'ils étaient au repos. Des individus âgés de 3 mois et 20-24 mois ( 4a ) ont servi de donneurs d'échantillons .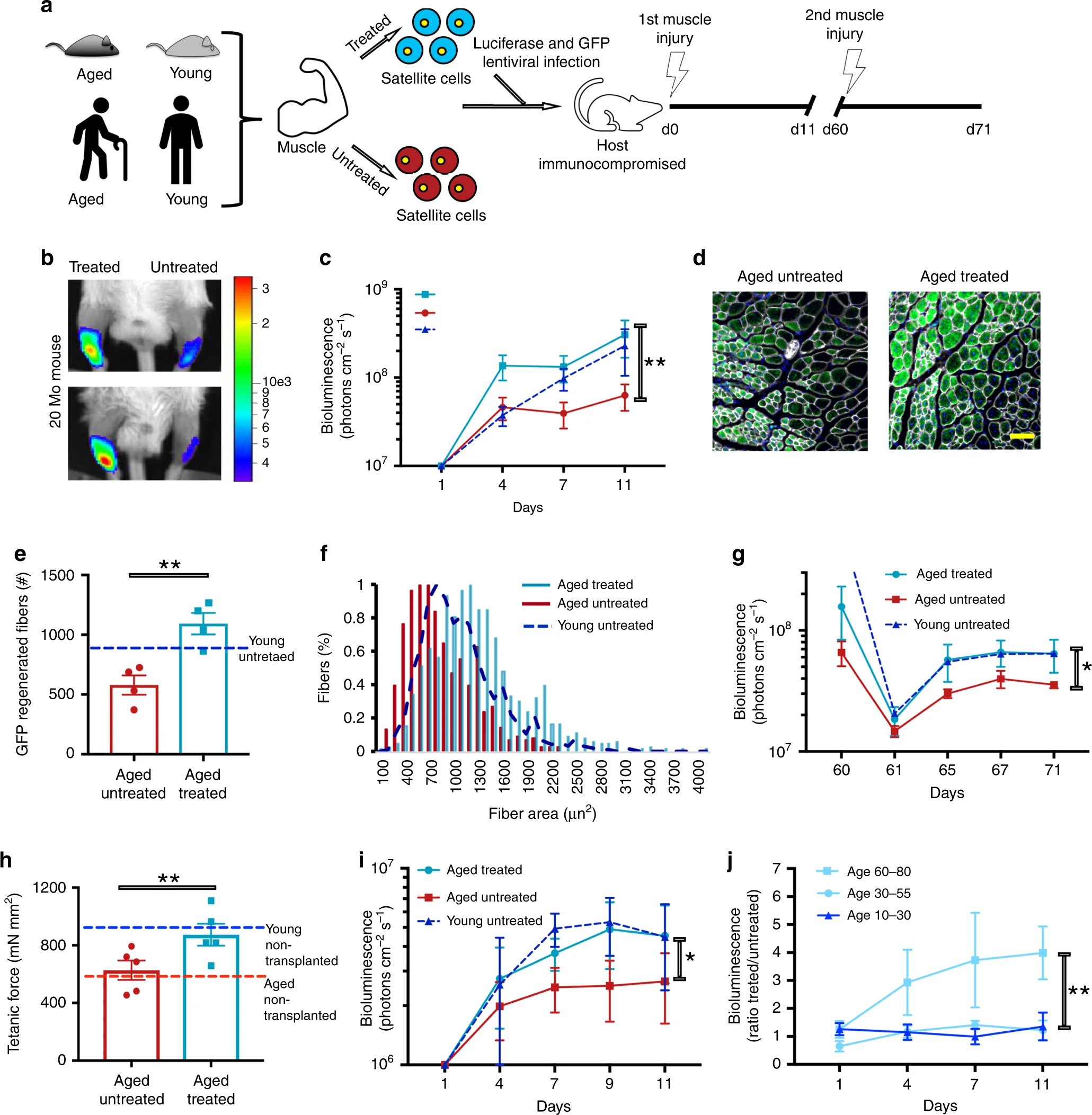 Image n ° 4 Letraitement de l'ancien MuSC a diminué à la fois le temps de la première division, s'approchant de la cinétique plus rapide d'activation des jeunes cellules MuSC et de la masse mitochondriale. De plus, la reprogrammation a partiellement restauré la capacité réduite de chaque MuSC à former des colonies.Ensuite, un test a été effectué sur la fonctionnalité et l'efficacité de MuSC en ce qui concerne la régénération de nouveaux tissus. Pour cela, la transduction de cellules MuSC jeunes, âgées ou temporairement reprogrammées a été réalisée en utilisant la luciférase exprimant les lentivirus et la GFP, qui ont ensuite été transplantées dans les muscles endommagés du tibia antérieur de souris immunodéprimées.L'imagerie bioluminescente a initialement montré que les muscles dans lesquels les MuSC reprogrammés étaient placés présentaient le signal le plus élevé (jour 4; 4b et 4c ). Cependant, au jour 11, ces muscles sont devenus similaires aux muscles où de jeunes MuSC ont été ajoutés. Mais les muscles où les cellules MuSC vieillissantes ont été ajoutées sans reprogrammation ont montré les signaux les plus faibles ( 4b et 4c)L'analyse par immunofluorescence a montré que les cellules avec reprogrammation fournissaient aux tissus plus de myofibrilles que les cellules sans traitement ( 4d et 4e ). 60 jours après la première analyse, une autre a été réalisée qui a montré les mêmes résultats ( 4g ). Cela indique directement une amélioration de la capacité de régénération des tissus après exposition à des cellules qui ont subi une reprogrammation.À l'étape suivante de l'étude, une attention particulière a été accordée aux modifications musculaires dégénératives atrophiques liées à l'âge. Les scientifiques ont décidé de vérifier si leur technique pouvait restaurer la force musculaire des souris âgées au niveau des jeunes.Tout d'abord, la force tétanique * a été établie dans les muscles des souris âgées de 4 et 27 mois.
Image n ° 4 Letraitement de l'ancien MuSC a diminué à la fois le temps de la première division, s'approchant de la cinétique plus rapide d'activation des jeunes cellules MuSC et de la masse mitochondriale. De plus, la reprogrammation a partiellement restauré la capacité réduite de chaque MuSC à former des colonies.Ensuite, un test a été effectué sur la fonctionnalité et l'efficacité de MuSC en ce qui concerne la régénération de nouveaux tissus. Pour cela, la transduction de cellules MuSC jeunes, âgées ou temporairement reprogrammées a été réalisée en utilisant la luciférase exprimant les lentivirus et la GFP, qui ont ensuite été transplantées dans les muscles endommagés du tibia antérieur de souris immunodéprimées.L'imagerie bioluminescente a initialement montré que les muscles dans lesquels les MuSC reprogrammés étaient placés présentaient le signal le plus élevé (jour 4; 4b et 4c ). Cependant, au jour 11, ces muscles sont devenus similaires aux muscles où de jeunes MuSC ont été ajoutés. Mais les muscles où les cellules MuSC vieillissantes ont été ajoutées sans reprogrammation ont montré les signaux les plus faibles ( 4b et 4c)L'analyse par immunofluorescence a montré que les cellules avec reprogrammation fournissaient aux tissus plus de myofibrilles que les cellules sans traitement ( 4d et 4e ). 60 jours après la première analyse, une autre a été réalisée qui a montré les mêmes résultats ( 4g ). Cela indique directement une amélioration de la capacité de régénération des tissus après exposition à des cellules qui ont subi une reprogrammation.À l'étape suivante de l'étude, une attention particulière a été accordée aux modifications musculaires dégénératives atrophiques liées à l'âge. Les scientifiques ont décidé de vérifier si leur technique pouvait restaurer la force musculaire des souris âgées au niveau des jeunes.Tout d'abord, la force tétanique * a été établie dans les muscles des souris âgées de 4 et 27 mois.Tétanos * - une condition de contraction musculaire prolongée.
Comme prévu, chez les souris plus âgées, cette force était significativement plus faible que chez les jeunes souris, ce qui indique un facteur d'âge ( 4h ).Ensuite, les cellules MuSC ont été isolées de souris âgées de 20 à 24 mois, qui ont ensuite subi un processus de reprogrammation, puis transplantées dans les muscles endommagés par la cardiotoxine de souris âgées de 20 mois. Après 30 jours, les mesures de force tétanique ont été répétées.Les muscles dans lesquels les cellules ont été transplantées sans reprogrammation ont montré les mêmes résultats que les muscles normaux de souris âgées sans aucune intervention. Mais les muscles où les cellules reprogrammées ont été placées ont montré des forces tétaniques comparables à celles des jeunes souris ( 4h ).Il s'ensuit que la reprogrammation temporaire en combinaison avec une thérapie à base de MuSC peut restaurer la fonction physiologique des muscles vieillissants aux fonctions des muscles jeunes.La réalisation d'une procédure similaire avec les muscles et les cellules humaines a montré des résultats positifs similaires ( 4i et 4j ).Pour une connaissance plus détaillée des nuances de l'étude, je vous recommande de consulter le rapport des scientifiques et les documents supplémentaires qui s'y rapportent.Épilogue
Dans l'étude que nous avons examinée aujourd'hui, les scientifiques ont pu démontrer une reprogrammation temporaire des cellules qui peut combattre les signes du vieillissement cellulaire et ne pas affecter l'identité cellulaire.Les cellules des personnes âgées qui ont subi une reprogrammation commencent à montrer les caractéristiques des jeunes cellules après quelques jours. Dans ce cas, l'effet persiste pendant six jours après l'arrêt du traitement.Cette technique est importante non seulement en termes de rajeunissement général des cellules et des tissus, mais aussi plus spécifiquement en ce qui concerne la lutte contre les effets des maladies liées à l'âge, telles que l'arthrose.À l'avenir, les scientifiques ont l'intention d'améliorer leur méthodologie. Premièrement, comme le disent les chercheurs eux-mêmes, il est nécessaire d'effectuer de nombreux tests en laboratoire et de vérifier pleinement la sécurité de la méthode au niveau cellulaire. Après cela, il sera possible de commencer son utilisation au niveau des tissus.L'humanité est-elle prête pour la jeunesse éternelle en termes de moralité, d'éthique et de psychologie? La question est complexe, mais elle a beaucoup de réponses. Cependant, le but de cette étude n'est pas dans la recherche de l'immortalité, mais dans la recherche de nouvelles méthodes efficaces de lutte contre diverses maladies qui surviennent en relation avec le vieillissement inévitable du corps. La vieillesse n'est pas aussi mauvaise que les maladies qui l'accompagnent. La même chose peut être dite à tout âge, car quelle joie y a-t-il dans la jeunesse éternelle mythique, si pendant toute cette éternité une personne lutte avec une plaie?Vendredi off-top:
, , , , . ( / Anastatica hierochuntica).
Merci de votre attention, restez curieux et passez un bon week-end à tous, les gars! :)Un peu de publicité :)
Merci de rester avec nous. Aimez-vous nos articles? Vous voulez voir des matériaux plus intéressants? Soutenez-nous en passant une commande ou en recommandant à vos amis, le cloud VPS pour les développeurs à partir de 4,99 $ , un analogue unique de serveurs d'entrée de gamme que nous avons inventé pour vous: Toute la vérité sur VPS (KVM) E5-2697 v3 (6 cœurs) 10 Go DDR4 480 Go SSD 1 Gbit / s à partir de 19 $ ou comment diviser le serveur? (les options sont disponibles avec RAID1 et RAID10, jusqu'à 24 cœurs et jusqu'à 40 Go de DDR4).Dell R730xd 2 fois moins cher au centre de données Equinix Tier IV à Amsterdam? Nous avons seulement 2 x Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 TV à partir de 199 $ aux Pays-Bas!Dell R420 - 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB - à partir de 99 $! En savoir plus sur la création d'un bâtiment d'infrastructure. classe c utilisant des serveurs Dell R730xd E5-2650 v4 coûtant 9 000 euros pour un sou?