 Dicen que la vida es un proceso continuo de envejecimiento, que inevitablemente termina en la muerte. Esto puede no parecer muy optimista, pero tales son las leyes de la naturaleza. El envejecimiento y la muerte son algunos de los reguladores más importantes de una población de cualquier tipo en el planeta, y la inmortalidad en el sentido biológico de la palabra existe solo en libros y películas. La misma situación es con la juventud "eterna". En los libros tenemos a Dorian Gray, un joven eternamente joven y guapo con una fuerte antipatía hacia una obra de arte en particular; Edward Cullen es un vampiro eternamente joven con deficiencia de vitamina D y alta reflectividad de la piel, etc. En realidad, la juventud eterna o al menos prolongada es inalcanzable. Al menos si los científicos no interfieren en el proceso. Hoy conoceremos el estudio,en el que los científicos de la Universidad de Stanford pudieron lograr el rejuvenecimiento de células humanas viejas debido a ciertas proteínas involucradas en el proceso de desarrollo embrionario. ¿Qué sustancias se usaron, qué edad tenían las células más jóvenes y cuánto tiempo fue el efecto? Aprendemos sobre esto del informe del grupo de investigación. Vamos.
Dicen que la vida es un proceso continuo de envejecimiento, que inevitablemente termina en la muerte. Esto puede no parecer muy optimista, pero tales son las leyes de la naturaleza. El envejecimiento y la muerte son algunos de los reguladores más importantes de una población de cualquier tipo en el planeta, y la inmortalidad en el sentido biológico de la palabra existe solo en libros y películas. La misma situación es con la juventud "eterna". En los libros tenemos a Dorian Gray, un joven eternamente joven y guapo con una fuerte antipatía hacia una obra de arte en particular; Edward Cullen es un vampiro eternamente joven con deficiencia de vitamina D y alta reflectividad de la piel, etc. En realidad, la juventud eterna o al menos prolongada es inalcanzable. Al menos si los científicos no interfieren en el proceso. Hoy conoceremos el estudio,en el que los científicos de la Universidad de Stanford pudieron lograr el rejuvenecimiento de células humanas viejas debido a ciertas proteínas involucradas en el proceso de desarrollo embrionario. ¿Qué sustancias se usaron, qué edad tenían las células más jóvenes y cuánto tiempo fue el efecto? Aprendemos sobre esto del informe del grupo de investigación. Vamos.Base de estudio
¿Qué es el envejecimiento? En esencia, este es un proceso de pérdida gradual de funcionalidad a nivel de moléculas, células, tejidos y todo el organismo.A nivel de cromatina * , el envejecimiento se asocia con una acumulación progresiva de errores epigenéticos * , que finalmente conducen a una regulación génica aberrante (anormal), agotamiento de células madre, envejecimiento y deterioro de la homeostasis de células / tejidos.Cromatina * : la base de los cromosomas, que consiste en ADN y proteínas (principalmente histonas). La cromatina se encuentra dentro del núcleo de las células eucariotas (organismos que tienen un núcleo en las células) y es parte del nucleoide en los procariotas (unicelulares sin núcleo).
Herencia epigenética * : un conjunto de cambios heredados en el fenotipo o la expresión génica.
Si aplica la reprogramación nuclear de las células de pluripotencia * , puede revertirla según su antigüedad, pero no su identidad.La pluripotencia * es una característica de una célula que puede diferenciarse en todos los tipos de células, excepto las células de los órganos extragérmenes.
Anteriormente, esta técnica ya se había probado en ratones. Los resultados fueron muy alentadores, ya que la reprogramación temporal mejoró las características de la edad y la vida útil prolongada en ratones. Pero el hombre no es un ratón y, por lo tanto, la cuestión sigue siendo cómo funcionará esta técnica en las células humanas. Esto es exactamente lo que los científicos están considerando en este estudio.El proceso de reprogramación nuclear en células madre pluripotentes inducidas ( iPSCs * ) se caracteriza por un restablecimiento completo (restablecimiento) de las características epigenéticas de las células, lo que conduce al retorno de la identidad celular y la edad a un estado similar al embrión.Las células madre pluripotentes inducidas (iPSC) * son un tipo de células madre obtenidas en el laboratorio a partir de células maduras diferenciadas de un organismo mamífero (incluidos los humanos).
Es curioso que la reprogramación no sea irreversible, deteniéndose en el llamado punto de no retorno (PNR desde el punto de no retorno), después de lo cual las células finalmente regresan a su estado somático * original .Célula somática * : células que forman el soma (cuerpo del cuerpo), pero que no participan en el desarrollo sexual.
Por lo tanto, si la reprogramación afectará a la célula durante un período de tiempo bastante corto, entonces la expresión de los factores de reprogramación no podrá borrar la firma epigenética que determina la identidad de las células. Resulta que una exposición corta no cambiará la identidad de la célula, pero ¿puede afectar su edad?La primera evidencia de que la reprogramación temporal puede mejorar los fenotipos durante el envejecimiento se mostró en ratones. Pero, como los científicos ya nos han recordado, los ratones no son humanos. Una pregunta importante de esta técnica es si puede funcionar en células humanas de origen natural aisladas de personas mayores.Para averiguarlo, los científicos realizaron una serie de experimentos para identificar el grado de impacto de la reprogramación nuclear en los fenotipos (signos externos e internos) de las células humanas y de ratón.Resultados de la investigacion
Primero, se realizó una evaluación del efecto de la expresión transitoria de los factores de reprogramación en la transcripción de dos tipos diferentes de células ( fibroblastos * y células endoteliales * ) en los ancianos. A continuación, se comparó la transcripción de los ancianos con la transcripción de los mismos tipos de células de donantes jóvenes ( 1a y 1e ).Fibroblastos * : células del tejido conectivo del cuerpo que sintetizan la matriz extracelular.
Endotelio * : una capa de células planas en las paredes internas de los vasos sanguíneos, los vasos linfáticos y las cavidades cardíacas.
 Imagen No. 1Se obtuvieron fibroblastos de muestras de biopsia * de la piel de las manos y el abdomen de los participantes del estudio: 3 personas de 25 a 35 años (grupo de jóvenes) y 8 personas de 60 a 90 años (grupo de ancianos).
Imagen No. 1Se obtuvieron fibroblastos de muestras de biopsia * de la piel de las manos y el abdomen de los participantes del estudio: 3 personas de 25 a 35 años (grupo de jóvenes) y 8 personas de 60 a 90 años (grupo de ancianos).Biopsia * : material biológico obtenido por biopsia.
Las células endoteliales se extrajeron de la vena ilíaca y la arteria de los participantes del estudio: 3 personas de 15 a 25 años (grupo de jóvenes) y 8 personas de 50 a 65 años (grupo de ancianos).Para los experimentos, se utilizó un protocolo de reprogramación no integrador, que se optimizó en base a un conjunto de ARNm que expresa las proteínas OCT4, SOX2, KLF4, c-MYC, LIN28 y NANOG.Este protocolo produce secuencialmente colonias de iPSC, independientemente de la edad de los donantes, después de 12-15 transfecciones diarias * .La transfección * es el proceso de introducción de ácido nucleico en células eucariotas por el método no viral.
Se encontró que el punto de no retorno en este caso se observa en el quinto día de reprogramación. Esta conclusión se basa en el hecho de que la primera expresión detectable de dcRNA * asociado a pluripotencia endógena ocurre el día 58.Los dnaRNA (ARN largos no codificantes) * son moléculas de ARN ubicadas en el núcleo o en el citoplasma que no se traducen en proteínas.
En vista de esto, se decidió usar un régimen temporal de expresión exógena en el que OSKMLN se transfectó diariamente durante 4 días consecutivos, y el análisis de expresión génica se realizó 2 días después de la interrupción ( 1b ).A continuación, se realizó una secuencia de ARN en masa para ambos tipos de células en los tres grupos de sujetos: jóvenes (Y), ancianos sin reprogramación (UA) y ancianos con reprogramación (TA).Para empezar, los científicos compararon las transcripciones normalizadas cuantiles de sujetos jóvenes y ancianos sin reprogramación (Y y UA). El análisis mostró que 961 genes (5.85%) en fibroblastos ( 1a y 1c ) y 748 genes (4.80%) en células endoteliales ( 1e y 1f) diferían entre células jóvenes y viejas.Estos conjuntos de genes están directamente relacionados con los procesos de envejecimiento. La determinación de la dirección de expresión por encima o por debajo del valor promedio de cada gen mostró una clara similitud entre las células de los jóvenes y las células de los ancianos después de la reprogramación de los fibroblastos y las células endoteliales ( 1d y 1g ).Usando el método descrito anteriormente, los científicos compararon las poblaciones celulares de sujetos ancianos con y sin reprogramación (TA y UA; 1a y 1e ). Se encontró que 1042 genes en fibroblastos y 992 en células endoteliales se expresaron diferencialmente.Estos perfiles de transcriptoma se utilizaron para confirmar la preservación de la identidad celular después de la reprogramación. El análisis mostró que no hubo cambios significativos en la identidad.En general, el análisis de las firmas de transcriptoma mostró que la expresión de OSKLMN promueve la activación muy rápida de un perfil de expresión génica más joven sin afectar la expresión del gen de identidad celular.Los investigadores señalan que los relojes epigenéticos * basados en los niveles de metilación del ADN * son los biomarcadores moleculares más precisos de la edad en tejidos y células. También predicen muchas afecciones relacionadas con la edad, incluida la esperanza de vida.* — , , .
* — .
También se sabe que la expresión exógena de factores de reprogramación canónica (OSKM) devuelve la edad epigenética de las células primarias al estado prenatal.Para comprobar si la expresión transitoria de OSKMLN puede revertir los relojes epigenéticos de las células somáticas humanas, los científicos utilizaron dos tipos de relojes epigenéticos que se aplican a los fibroblastos y células endoteliales humanas: el reloj epigenético original de Panvis Horvath (basado en 353 pares de citosina-fosfato-guanina) y relojes posteriores de "piel-sangre" (basados en 391 CpGs - sitios de moléculas de ADN).Calculadora de edad epigenética de HowarthSegún el reloj epigenético de Howart, la exposición temporal a OSKMLN revirtió significativamente la edad de la metilación del ADN (diferencia de edad media = -3,40 años). El efecto del rejuvenecimiento fue más pronunciado en las células endoteliales (diferencia de edad promedio = -4.94 años; 1i ) que en los fibroblastos (diferencia de edad promedio = -1.84; 1h ).Cualitativamente similares, pero se obtuvieron resultados menos significativos utilizando un reloj de piel-sangre: el efecto general del rejuvenecimiento es -1.35 años; El rejuvenecimiento promedio en las células endoteliales es -1.62 y en los fibroblastos -1.07.En base a estos resultados, se realizó un análisis del efecto de la reprogramación temporal en varios signos de envejecimiento fisiológico celular. Para ello, se realizó la visualización de células individuales y una extensa base de datos de signos de envejecimiento.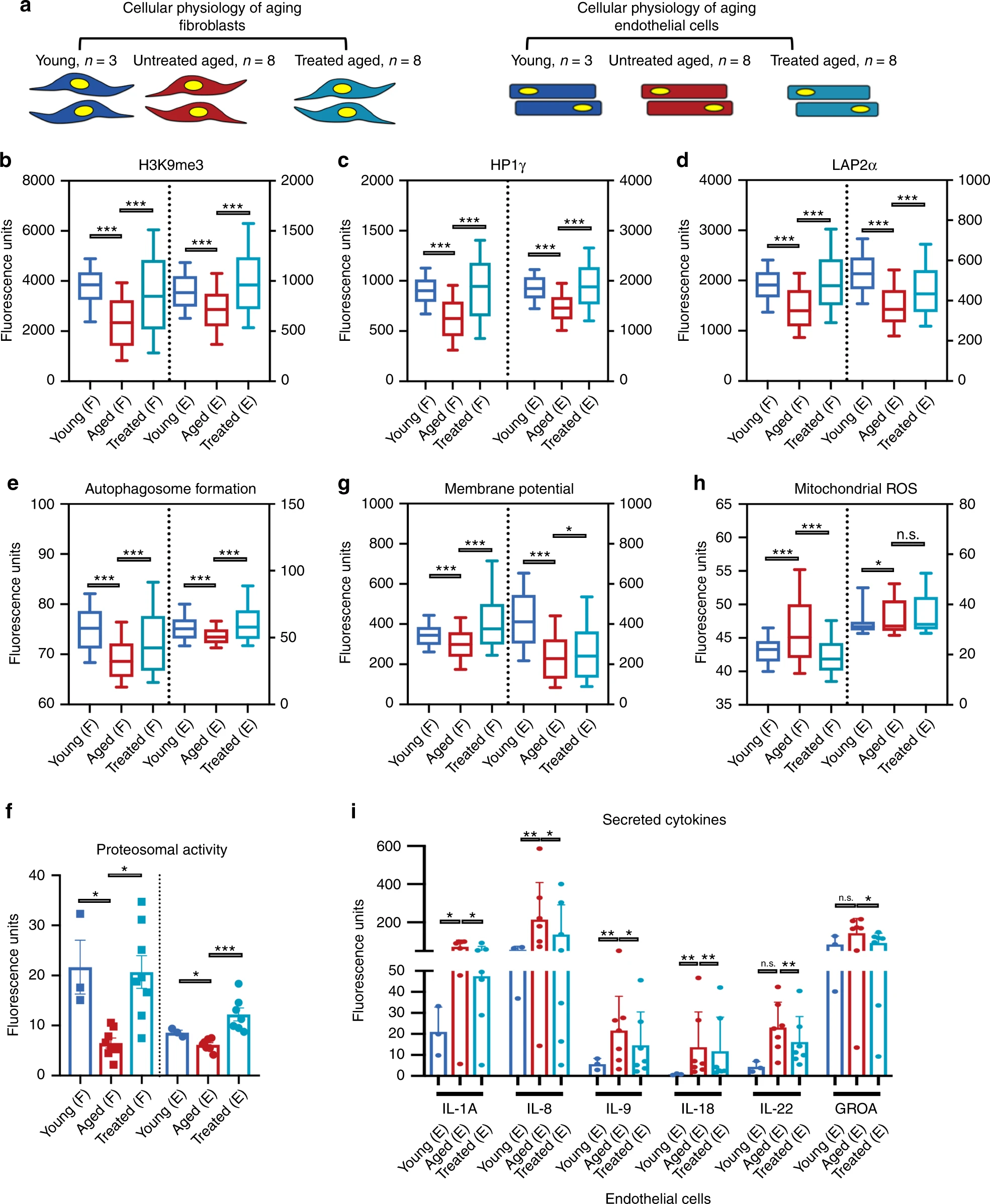 Imagen No. 2Todos los análisis se llevaron a cabo por separado en cada línea celular separada ( 2a ): 19 líneas de fibroblastos (3 - jóvenes, 8 - ancianos y 8 - ancianos después de la reprogramación) y 17 líneas de células endoteliales (3 - jóvenes, 7 - ancianos y 7 - ancianos después de la reprogramación). El análisis estadístico se realizó mediante muestreo aleatorio de 100 células por muestra.Para ampliar los resultados anteriores sobre epigenética, se realizaron mediciones cuantitativas adicionales utilizando inmunofluorescencia (IF) de la etiqueta represiva epigenética H3K9me3, la proteína HP1γ asociada a la heterocromatina y la proteína LAP2α que apoya la laminina nuclear * ( 2b - 2d ).
Imagen No. 2Todos los análisis se llevaron a cabo por separado en cada línea celular separada ( 2a ): 19 líneas de fibroblastos (3 - jóvenes, 8 - ancianos y 8 - ancianos después de la reprogramación) y 17 líneas de células endoteliales (3 - jóvenes, 7 - ancianos y 7 - ancianos después de la reprogramación). El análisis estadístico se realizó mediante muestreo aleatorio de 100 células por muestra.Para ampliar los resultados anteriores sobre epigenética, se realizaron mediciones cuantitativas adicionales utilizando inmunofluorescencia (IF) de la etiqueta represiva epigenética H3K9me3, la proteína HP1γ asociada a la heterocromatina y la proteína LAP2α que apoya la laminina nuclear * ( 2b - 2d ).Nuclear Lamin * : una red rígida fibrilar debajo de la membrana nuclear, que participa en la organización de la cromatina.
Como se informó anteriormente en estudios anteriores, en fibroblastos maduros y células endoteliales, se observó una disminución en la señal nuclear para los tres marcadores en comparación con las células jóvenes. La reprogramación de las células más antiguas ha llevado a un aumento de estos marcadores en ambos tipos de células.A continuación, se estudió la actividad proteolítica (hidrólisis de proteínas) de las células midiendo la formación de autofagosomas, y también se estudió la actividad del proteasoma similar a la quimotripsina. La reprogramación no solo aumentó ambos tipos de actividad al nivel de las células jóvenes, sino que también la excedió ( 2e y 2f ). Esto sugiere que las primeras etapas de la reprogramación contribuyen a la eliminación activa de biomoléculas degradadas.Uno de los signos más indicativos del envejecimiento celular es la disminución de la actividad mitocondrial, la acumulación de especies reactivas de oxígeno (ROS) y la desregulación de la sensibilidad a los nutrientes. Por lo tanto, es posible verificar el efecto de la reprogramación en las células envejecidas midiendo el potencial de membrana de las mitocondrias, las mitocondrias ROS y los niveles de proteínas de Sirtuin1 (SIRT1).La reprogramación temporal aumentó el potencial de membrana de las mitocondrias en ambos tipos de células ( 2 g ), disminuyó las ROS mitocondriales ( 2 h ) y aumentó los niveles de proteína SIRT1 en los fibroblastos, lo que se observa en las células jóvenes.La obtención de imágenes celulares mediante la tinción de beta-galactosidasa asociada con el envejecimiento mostró una disminución significativa en el número de células envejecidas en las células endoteliales, pero no en los fibroblastos. Esto fue acompañado por una disminución en la cantidad de citocinas fenotípicas secretoras asociadas con el envejecimiento proinflamatorio, y nuevamente en las células endoteliales, pero no en los fibroblastos ( 2i ).También se encontró que en ninguno de los tipos de células la longitud de los telómeros * muestra un alargamiento significativo después de la reprogramación. Esto puede indicar que las células no se diferencian en un estado similar a las células madre cuando se reactiva la actividad de la telomerasa * .* — .
* — , 3'- .
También se encontró que los efectos de la reprogramación en las células persistieron incluso después de 4 y 6 días después de que este proceso se detuvo. Desde el punto de vista de la velocidad de manifestación de los efectos de la reprogramación, se observaron ya 2 días después del inicio de este proceso.En total, estos datos sugieren que la expresión transitoria de OSKMLN puede causar una mejora y un cambio rápidos y continuos en la edad celular en células somáticas humanas a nivel transcriptómico, epigenético y celular. Además, este rejuvenecimiento se produce en las primeras etapas de la reprogramación, por lo que esta técnica no tiene tiempo para afectar la identidad de las células.Luego, los científicos decidieron averiguar si la expresión transitoria de OSKMNL también podría revertir los fenotipos inflamatorios asociados con el envejecimiento. Después de obtener evidencia preliminar de este cambio en las células endoteliales ( 2j ), el análisis se expandió agregando osteoartritis, una enfermedad fuertemente asociada con el envejecimiento y caracterizada por un pronunciado proceso inflamatorio que afecta a los condrocitos en las articulaciones.Se tomaron muestras: condrocitos del cartílago de seis pacientes de 60 a 70 años que se sometieron a una operación completa de reemplazo articular debido a una osteoartritis en etapa tardía. Además, estas muestras se reprogramaron y los resultados se compararon con los datos de condrocitos de tres jóvenes ( 3a ). Imagen No. 3La expresión temporal de OSKMLN se realizó durante 2 o 3 días y el análisis se realizó 2 días después de la interrupción de la reprogramación, aunque los pacientes tuvieron un efecto más duradero con un tratamiento más prolongado.Sin embargo, el uso de OSKMLN mostró una disminución significativa en los niveles de ARNm intracelular de RANKL (citocina de la familia de los factores de necrosis tumoral) e iNOS2, así como los niveles de factores inflamatorios secretados por las células ( 3b - 3d ).Además, se observó un aumento en la proliferación celular ( 3e ), un aumento en la producción de ATP ( 3f ) y una disminución en el proceso oxidativo ( 3g y 3h ).La verificación de la identidad celular mostró que el proceso de reprogramación no lo violó: no hubo efecto sobre el nivel de expresión de SOX9, y el nivel de expresión de COL2A1 aumentó significativamente (qRT-PCR en 3i y 3j ).De los resultados anteriores se deduce que la expresión transitoria de OSKMLN puede contribuir a una reversión parcial de la expresión génica y la fisiología celular en condrocitos más viejos con osteoartritis a un estado más joven. Por lo tanto, la técnica estudiada también puede usarse como uno de los métodos para tratar la osteoartritis en los ancianos.Otro signo importante del envejecimiento es la pérdida de la función de las células madre y la pérdida de la capacidad regenerativa. Para probar el efecto de la reprogramación en estos factores, los científicos utilizaron células madre de músculo esquelético de ratón (MuSC).Los MuSC estuvieron expuestos a la reprogramación durante 2 días mientras estaban en reposo. Las personas de 3 meses y 20-24 meses ( 4a ) sirvieron como donantes de muestra .
Imagen No. 3La expresión temporal de OSKMLN se realizó durante 2 o 3 días y el análisis se realizó 2 días después de la interrupción de la reprogramación, aunque los pacientes tuvieron un efecto más duradero con un tratamiento más prolongado.Sin embargo, el uso de OSKMLN mostró una disminución significativa en los niveles de ARNm intracelular de RANKL (citocina de la familia de los factores de necrosis tumoral) e iNOS2, así como los niveles de factores inflamatorios secretados por las células ( 3b - 3d ).Además, se observó un aumento en la proliferación celular ( 3e ), un aumento en la producción de ATP ( 3f ) y una disminución en el proceso oxidativo ( 3g y 3h ).La verificación de la identidad celular mostró que el proceso de reprogramación no lo violó: no hubo efecto sobre el nivel de expresión de SOX9, y el nivel de expresión de COL2A1 aumentó significativamente (qRT-PCR en 3i y 3j ).De los resultados anteriores se deduce que la expresión transitoria de OSKMLN puede contribuir a una reversión parcial de la expresión génica y la fisiología celular en condrocitos más viejos con osteoartritis a un estado más joven. Por lo tanto, la técnica estudiada también puede usarse como uno de los métodos para tratar la osteoartritis en los ancianos.Otro signo importante del envejecimiento es la pérdida de la función de las células madre y la pérdida de la capacidad regenerativa. Para probar el efecto de la reprogramación en estos factores, los científicos utilizaron células madre de músculo esquelético de ratón (MuSC).Los MuSC estuvieron expuestos a la reprogramación durante 2 días mientras estaban en reposo. Las personas de 3 meses y 20-24 meses ( 4a ) sirvieron como donantes de muestra .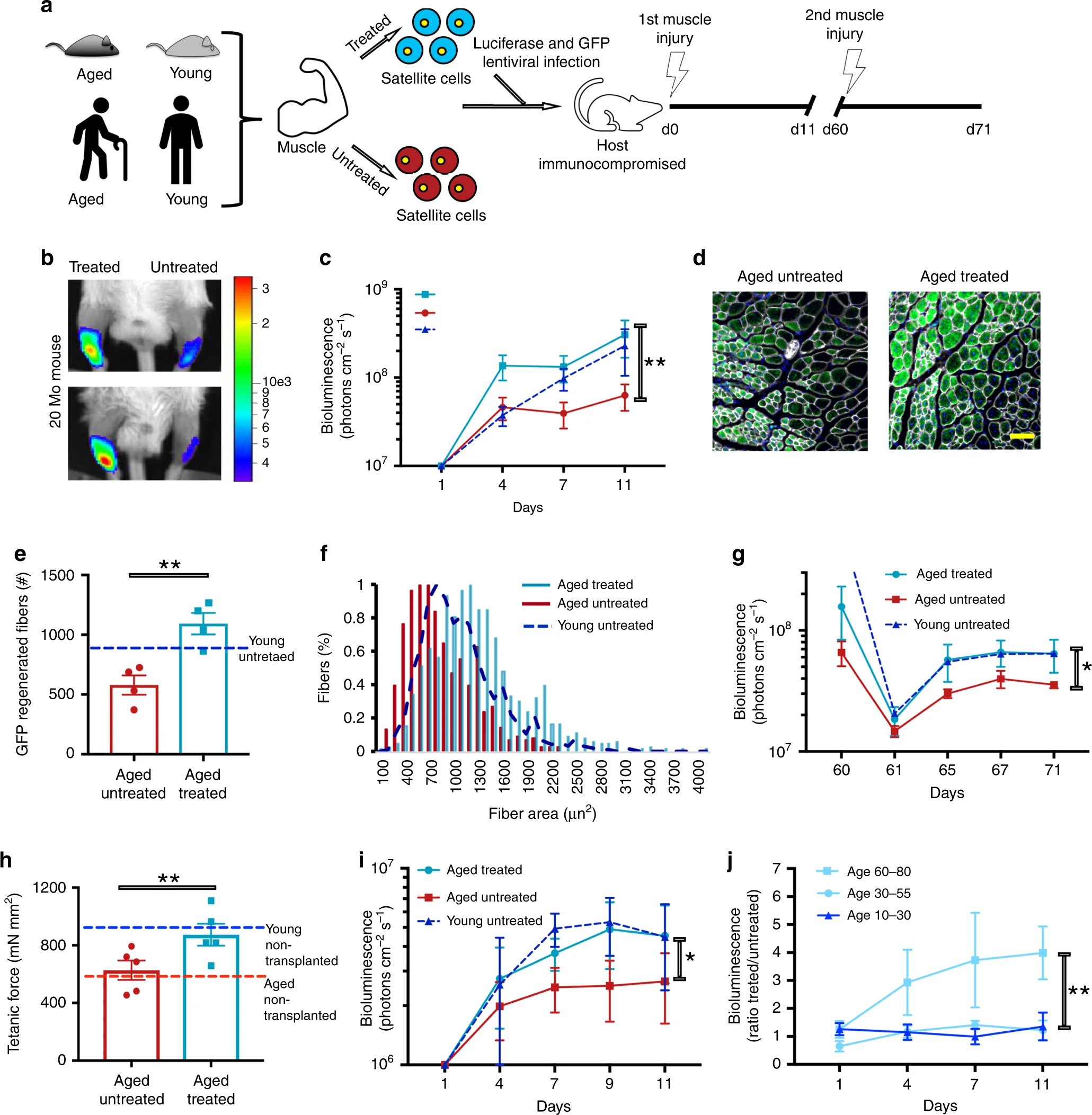 Imagen No. 4 Elprocesamiento de MuSC antiguo disminuyó tanto el tiempo de la primera división, acercándose a la cinética más rápida de activación de las células MuSC jóvenes, como a la masa mitocondrial. Además, la reprogramación restauró parcialmente la capacidad reducida de MuSC individuales para formar colonias.A continuación, se realizó una prueba de la funcionalidad y efectividad de MuSC con respecto a la regeneración de tejido nuevo. Para esto, se realizó la transducción de células MuSC jóvenes, de edad avanzada o reprogramadas temporalmente utilizando luciferasa que expresa lentivirus y GFP, que luego se trasplantaron a músculos dañados de la tibia anterior de ratones inmunocomprometidos.Las imágenes bioluminiscentes mostraron inicialmente que los músculos en los que se colocaron los MuSC reprogramados mostraron la señal más alta (día 4; 4b y 4c ). Sin embargo, en el día 11, estos músculos se volvieron similares a los músculos donde se agregaron MuSC jóvenes. Pero los músculos donde se añadieron las células MuSC envejecidas sin reprogramación mostraron las señales más débiles ( 4b y 4c)El análisis de inmunofluorescencia mostró que las células con reprogramación proporcionaron a los tejidos más miofibrillas que las células sin tratamiento ( 4d y 4e ). 60 días después del primer análisis, se realizó otro que mostró los mismos resultados ( 4 g ). Esto indica directamente una mejora en la capacidad regenerativa de los tejidos después de la exposición a las células que han sido reprogramadas.En la siguiente etapa del estudio, se prestó especial atención a los cambios musculares degenerativos atróficos relacionados con la edad. Los científicos decidieron verificar si su técnica puede restaurar la fuerza muscular de los ratones mayores al nivel de los jóvenes.Primero, se estableció la fuerza tetánica * en los músculos de ratones de 4 y 27 meses.
Imagen No. 4 Elprocesamiento de MuSC antiguo disminuyó tanto el tiempo de la primera división, acercándose a la cinética más rápida de activación de las células MuSC jóvenes, como a la masa mitocondrial. Además, la reprogramación restauró parcialmente la capacidad reducida de MuSC individuales para formar colonias.A continuación, se realizó una prueba de la funcionalidad y efectividad de MuSC con respecto a la regeneración de tejido nuevo. Para esto, se realizó la transducción de células MuSC jóvenes, de edad avanzada o reprogramadas temporalmente utilizando luciferasa que expresa lentivirus y GFP, que luego se trasplantaron a músculos dañados de la tibia anterior de ratones inmunocomprometidos.Las imágenes bioluminiscentes mostraron inicialmente que los músculos en los que se colocaron los MuSC reprogramados mostraron la señal más alta (día 4; 4b y 4c ). Sin embargo, en el día 11, estos músculos se volvieron similares a los músculos donde se agregaron MuSC jóvenes. Pero los músculos donde se añadieron las células MuSC envejecidas sin reprogramación mostraron las señales más débiles ( 4b y 4c)El análisis de inmunofluorescencia mostró que las células con reprogramación proporcionaron a los tejidos más miofibrillas que las células sin tratamiento ( 4d y 4e ). 60 días después del primer análisis, se realizó otro que mostró los mismos resultados ( 4 g ). Esto indica directamente una mejora en la capacidad regenerativa de los tejidos después de la exposición a las células que han sido reprogramadas.En la siguiente etapa del estudio, se prestó especial atención a los cambios musculares degenerativos atróficos relacionados con la edad. Los científicos decidieron verificar si su técnica puede restaurar la fuerza muscular de los ratones mayores al nivel de los jóvenes.Primero, se estableció la fuerza tetánica * en los músculos de ratones de 4 y 27 meses.Tétanos * : una condición de contracción muscular prolongada.
Como se esperaba, en ratones mayores esta fuerza fue significativamente menor que en ratones jóvenes, lo que indica un factor de edad ( 4h ).Luego, se aislaron células MuSC de ratones de entre 20 y 24 meses, que luego se sometieron a un proceso de reprogramación, y luego se trasplantaron en el músculo dañado por cardiotoxina de ratones de 20 meses. Después de 30 días, se repitieron las mediciones de resistencia tetánica.Los músculos en los que se trasplantaron las células sin reprogramación mostraron los mismos resultados que los músculos normales de ratones ancianos sin ninguna intervención. Pero los músculos donde se colocaron las células con reprogramación mostraron fuerzas tetánicas comparables a los músculos de ratones jóvenes ( 4h ).De ello se deduce que la reprogramación temporal en combinación con la terapia basada en MuSC puede restaurar la función fisiológica de los músculos que envejecen a las funciones de los músculos jóvenes.La realización de un procedimiento similar con músculos y células humanas mostró resultados positivos similares ( 4i y 4j ).Para un conocimiento más detallado de los matices del estudio, le recomiendo que consulte el informe de los científicos y materiales adicionales .Epílogo
En el estudio que examinamos hoy, los científicos pudieron demostrar una reprogramación temporal de células que pueden combatir los signos del envejecimiento celular y no afectar la identidad celular.Las células de las personas mayores que han sido reprogramadas comienzan a demostrar las características de las células jóvenes después de unos días. En este caso, el efecto persiste durante seis días después de la interrupción del tratamiento.Esta técnica es importante no solo en términos del rejuvenecimiento general de células y tejidos, sino también más específicamente en el aspecto de combatir los efectos de enfermedades relacionadas con la edad, como la osteoartritis.En el futuro, los científicos tienen la intención de mejorar su metodología. En primer lugar, como dicen los propios investigadores, es necesario realizar muchas pruebas en el laboratorio y verificar completamente la seguridad del método a nivel celular. Después de eso, será posible comenzar su uso a nivel de tejido.¿Está lista la humanidad para la eterna juventud en términos de moralidad, ética y psicología? La pregunta es compleja, pero tiene muchas respuestas. Sin embargo, el propósito de este estudio no es la búsqueda de la inmortalidad, sino la búsqueda de nuevos métodos efectivos para combatir diversas enfermedades que surgen en relación con el inevitable envejecimiento del cuerpo. La vejez no es tan mala como las enfermedades que la acompañan. Lo mismo puede decirse de cualquier edad, ¿qué alegría hay en la mítica juventud eterna, si por toda esta eternidad una persona luchara con alguna llaga?Viernes off-top:
, , , , . ( / Anastatica hierochuntica).
¡Gracias por su atención, tengan curiosidad y tengan un gran fin de semana a todos, muchachos! :)Un poco de publicidad :)
Gracias por estar con nosotros. ¿Te gustan nuestros artículos? ¿Quieres ver más materiales interesantes? Apóyenos haciendo un pedido o recomendando a sus amigos, VPS en la nube para desarrolladores desde $ 4.99 , un análogo único de servidores de nivel básico que inventamos para usted: toda la verdad sobre VPS (KVM) E5-2697 v3 (6 núcleos) 10GB DDR4 480GB SSD 1Gbps desde $ 19 o cómo dividir el servidor? (las opciones están disponibles con RAID1 y RAID10, hasta 24 núcleos y hasta 40GB DDR4).Dell R730xd 2 veces más barato en el centro de datos Equinix Tier IV en Amsterdam? ¡Solo tenemos 2 x Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 TV desde $ 199 en los Países Bajos!Dell R420 - 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB - ¡desde $ 99! Lea sobre Cómo construir un edificio de infraestructura. clase c con servidores Dell R730xd E5-2650 v4 que cuestan 9,000 euros por un centavo?