 Sie sagen, dass das Leben ein kontinuierlicher Alterungsprozess ist, der unweigerlich zum Tod führt. Das mag nicht sehr optimistisch klingen, aber das sind die Naturgesetze. Altern und Tod sind einige der wichtigsten Regulatoren einer Bevölkerung jeglicher Art auf dem Planeten, und Unsterblichkeit im biologischen Sinne des Wortes gibt es nur in Büchern und Filmen. Die gleiche Situation ist mit "ewiger" Jugend. In den Büchern haben wir Dorian Gray - einen ewig jungen und gutaussehenden jungen Mann mit einer starken Abneigung gegen ein bestimmtes Kunstwerk; Edward Cullen ist ein ewig junger Vampir mit Vitamin D-Mangel und hohem Hautreflexionsvermögen usw. In Wirklichkeit ist eine ewige oder zumindest verlängerte Jugend unerreichbar. Zumindest wenn sich Wissenschaftler nicht in den Prozess einmischen. Heute werden wir die Studie kennenlernen,in denen Wissenschaftler der Stanford University aufgrund bestimmter Proteine, die am Prozess der Embryonalentwicklung beteiligt sind, eine Verjüngung alter menschlicher Zellen erreichen konnten. Welche Substanzen wurden verwendet, wie alt waren die Zellen jünger und wie lange war die Wirkung? Dies erfahren wir aus dem Bericht der Forschungsgruppe. Gehen.
Sie sagen, dass das Leben ein kontinuierlicher Alterungsprozess ist, der unweigerlich zum Tod führt. Das mag nicht sehr optimistisch klingen, aber das sind die Naturgesetze. Altern und Tod sind einige der wichtigsten Regulatoren einer Bevölkerung jeglicher Art auf dem Planeten, und Unsterblichkeit im biologischen Sinne des Wortes gibt es nur in Büchern und Filmen. Die gleiche Situation ist mit "ewiger" Jugend. In den Büchern haben wir Dorian Gray - einen ewig jungen und gutaussehenden jungen Mann mit einer starken Abneigung gegen ein bestimmtes Kunstwerk; Edward Cullen ist ein ewig junger Vampir mit Vitamin D-Mangel und hohem Hautreflexionsvermögen usw. In Wirklichkeit ist eine ewige oder zumindest verlängerte Jugend unerreichbar. Zumindest wenn sich Wissenschaftler nicht in den Prozess einmischen. Heute werden wir die Studie kennenlernen,in denen Wissenschaftler der Stanford University aufgrund bestimmter Proteine, die am Prozess der Embryonalentwicklung beteiligt sind, eine Verjüngung alter menschlicher Zellen erreichen konnten. Welche Substanzen wurden verwendet, wie alt waren die Zellen jünger und wie lange war die Wirkung? Dies erfahren wir aus dem Bericht der Forschungsgruppe. Gehen.Studienbasis
Was ist Altern? Im Kern handelt es sich hierbei um einen Prozess des allmählichen Funktionsverlusts auf der Ebene von Molekülen, Zellen, Geweben und dem gesamten Organismus.Auf Chromatin * -Ebene ist das Altern mit einer fortschreitenden Anhäufung epigenetischer * Fehler verbunden, die letztendlich zu einer aberranten (abnormalen) Genregulation, Stammzellverarmung, Alterung und einer beeinträchtigten Zell / Gewebe-Homöostase führen.Chromatin * - die Basis von Chromosomen, bestehend aus DNA und Proteinen (meist Histonen). Chromatin befindet sich im Kern von eukaryotischen Zellen (Organismen, die einen Kern in den Zellen haben) und ist Teil des Nukleoids in Prokaryoten (einzellig ohne Kern).
Epigenetische Vererbung * - eine Reihe von vererbten Veränderungen des Phänotyps oder der Genexpression.
Wenn Sie die nukleare Reprogrammierung von Pluripotenz * -Zellen anwenden , können Sie sie als Alter, aber nicht als Identität umkehren.Pluripotenz * ist ein Merkmal einer Zelle, die sich in alle Zelltypen mit Ausnahme von Zellen von Extrakeimorganen unterscheiden kann.
Zuvor wurde diese Technik bereits an Mäusen getestet. Die Ergebnisse waren sehr ermutigend, da die vorübergehende Neuprogrammierung die Alterseigenschaften verbesserte und die Lebensdauer bei Mäusen verlängerte. Aber der Mensch ist keine Maus, und daher bleibt die Frage, wie diese Technik auf menschliche Zellen wirken wird. Genau das berücksichtigen Wissenschaftler in dieser Studie.Der Prozess der nuklearen Reprogrammierung in induzierte pluripotente Stammzellen ( iPSCs * ) ist durch ein vollständiges Dumping (Nachladen) der epigenetischen Eigenschaften von Zellen gekennzeichnet, was zur Rückkehr sowohl der zellulären Identität als auch des Alters in den embryoähnlichen Zustand führt.Induzierte pluripotente Stammzellen (iPSCs) * sind eine Art von Stammzellen, die im Labor aus reifen differenzierten Zellen eines Säugetierorganismus (einschließlich Menschen) gewonnen werden.
Es ist merkwürdig, dass die Neuprogrammierung nicht irreversibel ist und bis zum sogenannten Punkt ohne Rückkehr (PNR ab Punkt ohne Rückkehr) anhält, wonach die Zellen schließlich in ihren ursprünglichen somatischen Zustand zurückkehren.Somatische Zelle * - Zellen, die das Soma (Körper des Körpers) bilden, aber nicht an der sexuellen Entwicklung beteiligt sind.
Wenn daher die Reprogrammierung die Zelle für einen relativ kurzen Zeitraum beeinflusst, kann die Expression von Reprogrammierungsfaktoren die epigenetische Signatur, die die Identität der Zellen bestimmt, nicht löschen. Es stellt sich heraus, dass eine kurze Exposition die Identität der Zelle nicht verändert, aber kann sie ihr Alter beeinflussen?Der erste Beweis, dass eine vorübergehende Reprogrammierung die Phänotypen während des Alterns verbessern kann, wurde bei Mäusen gezeigt. Aber, wie uns Wissenschaftler bereits erinnert haben, sind Mäuse keine Menschen. Eine wichtige Frage dieser Technik ist, ob sie auf natürlich vorkommende menschliche Zellen wirken kann, die von älteren Menschen isoliert wurden.Um dies herauszufinden, führten die Wissenschaftler eine Reihe von Experimenten durch, um den Grad der Auswirkung der nuklearen Reprogrammierung auf die Phänotypen (äußere und innere Zeichen) von menschlichen und Mauszellen zu bestimmen.Forschungsergebnisse
Zunächst wurde die Auswirkung der vorübergehenden Expression von Reprogrammierungsfaktoren auf das Transkript von zwei verschiedenen Zelltypen ( Fibroblasten * und Endothelzellen * ) bei älteren Menschen bewertet . Als nächstes wurde das Transkript älterer Menschen mit dem Transkript derselben Zelltypen junger Spender ( 1a und 1e ) verglichen .Fibroblasten * - Zellen des Bindegewebes des Körpers, die die extrazelluläre Matrix synthetisieren.
Endothel * - eine Schicht flacher Zellen an den Innenwänden von Blutgefäßen, Lymphgefäßen und Herzhöhlen.
 Bild Nr. 1Fibroblasten wurden aus Biopsieproben * der Haut von Händen und Bauch der Studienteilnehmer erhalten: 3 Personen im Alter von 25 bis 35 Jahren (junge Gruppe) und 8 Personen im Alter von 60 bis 90 Jahren (ältere Gruppe).
Bild Nr. 1Fibroblasten wurden aus Biopsieproben * der Haut von Händen und Bauch der Studienteilnehmer erhalten: 3 Personen im Alter von 25 bis 35 Jahren (junge Gruppe) und 8 Personen im Alter von 60 bis 90 Jahren (ältere Gruppe).Biopsie * - durch Biopsie gewonnenes biologisches Material.
Endothelzellen wurden aus der Iliakalvene und der Arterie der Studienteilnehmer extrahiert: 3 Personen im Alter von 15 bis 25 Jahren (junge Gruppe) und 8 Personen im Alter von 50 bis 65 Jahren (ältere Gruppe).Für die Experimente wurde ein nicht integratives Reprogrammierungsprotokoll verwendet, das basierend auf einem Satz von mRNA optimiert wurde, die OCT4-, SOX2-, KLF4-, c-MYC-, LIN28- und NANOG-Proteine exprimieren.Dieses Protokoll erzeugt nach 12–15 täglichen Transfektionen * nacheinander iPSC-Kolonien, unabhängig vom Alter der Spender .Transfektion * ist der Prozess der Einführung von Nukleinsäure in eukaryotische Zellen nach der nicht-viralen Methode.
Es wurde festgestellt, dass der Punkt, an dem in diesem Fall keine Rückkehr erfolgt, am fünften Tag der Neuprogrammierung beobachtet wird. Diese Schlussfolgerung basiert auf der Tatsache, dass die erste nachweisbare Expression von endogener pluripotenzassoziierter dcRNA * am Tag 58 erfolgt.dnaRNAs (lange nicht-kodierende RNAs) * sind RNA-Moleküle im Zellkern oder im Zytoplasma, die nicht in Proteine übersetzt werden.
In Anbetracht dessen wurde beschlossen, ein temporäres Regime der exogenen Expression zu verwenden, bei dem OSKMLN an 4 aufeinanderfolgenden Tagen täglich transfiziert wurde und die Genexpressionsanalyse 2 Tage nach der Unterbrechung durchgeführt wurde ( 1b ).Als nächstes wurde eine gepaarte Massen-RNA-Sequenzierung für beide Zelltypen in allen drei Gruppen von Probanden durchgeführt: jung (Y), ältere Menschen ohne Neuprogrammierung (UA) und ältere Menschen mit Neuprogrammierung (TA).Zunächst verglichen die Wissenschaftler die quantilnormalisierten Transkripte junger Probanden und älterer Menschen ohne Neuprogrammierung (Y und UA). Die Analyse zeigte, dass 961 Gene (5,85%) in Fibroblasten ( 1a und 1c ) und 748 Gene (4,80%) in Endothelzellen ( 1e und 1f)) unterschieden sich zwischen jungen und alten Zellen.Diese Gensätze stehen in direktem Zusammenhang mit Alterungsprozessen. Die Bestimmung der Expressionsrichtung über oder unter dem Durchschnittswert jedes Gens zeigte eine deutliche Ähnlichkeit zwischen den Zellen junger Menschen und den Zellen älterer Menschen nach Reprogrammierung sowohl für Fibroblasten als auch für Endothelzellen ( 1d und 1g ).Unter Verwendung der oben beschriebenen Methode verglichen die Wissenschaftler die Zellpopulationen älterer Probanden mit und ohne Neuprogrammierung (TA und UA; 1a und 1e ). Es wurde gefunden, dass 1042 Gene in Fibroblasten und 992 in Endothelzellen unterschiedlich exprimiert wurden.Diese Transkriptomprofile wurden dann verwendet, um die Erhaltung der Zellidentität nach der Reprogrammierung zu bestätigen. Die Analyse zeigte, dass es keine signifikanten Identitätsänderungen gab.Im Allgemeinen zeigte die Analyse von Transkriptomsignaturen, dass die OSKLMN-Expression eine sehr schnelle Aktivierung eines jüngeren Genexpressionsprofils fördert, ohne die Genexpression der Zellidentität zu beeinflussen.Die Forscher stellen fest, dass epigenetische Uhren * basierend auf DNA-Methylierungsniveaus * die genauesten molekularen Biomarker des Alters in Geweben und Zellen sind. Sie sagen auch viele altersbedingte Zustände voraus, einschließlich der Lebenserwartung.* — , , .
* — .
Es ist auch bekannt, dass die exogene Expression kanonischer Reprogrammierungsfaktoren (OSKM) das epigenetische Alter der Primärzellen in den pränatalen Zustandzurückversetzt . Um zu testen, ob die vorübergehende Expression von OSKMLN die epigenetischen Uhren menschlicher Körperzellen umkehren kann, verwendeten die Wissenschaftler zwei Arten epigenetischer Uhren, die für Fibroblasten und menschliche Endothelzellen: die ursprüngliche epigenetische Uhr von Panvis Horvath (basierend auf 353 Paaren Cytosin-Phosphat-Guanin) und später „Haut-Blut“ -Uhren (basierend auf 391 CpGs - Abschnitte des DNA-Moleküls).Howarth Epigenetic Age CalculatorLaut Howarts epigenetischer Uhr kehrte die vorübergehende Exposition gegenüber OSKMLN das Alter der DNA-Methylierung signifikant um (mittlerer Altersunterschied = -3,40 Jahre). ; Die Wirkung der Verjüngung mehr wurde in Endothelzellen (durchschnittliche Altersunterschied = -4,94 Jahre ausgesprochen 1i als in Fibroblasten (durchschnittliche Altersunterschied = -1,84;) 1h ).Qualitativ ähnliche, aber weniger signifikante Ergebnisse wurden unter Verwendung einer Haut-Blut-Uhr erhalten: Der Gesamteffekt der Verjüngung beträgt -1,35 Jahre; Die durchschnittliche Verjüngung in Endothelzellen beträgt -1,62 und in Fibroblasten -1,07.Basierend auf diesen Ergebnissen wurde eine Analyse der Auswirkung einer vorübergehenden Neuprogrammierung auf verschiedene Anzeichen einer zellphysiologischen Alterung durchgeführt. Hierzu wurden die Visualisierung einzelner Zellen und eine umfangreiche Datenbank mit Zeichen des Alterns durchgeführt.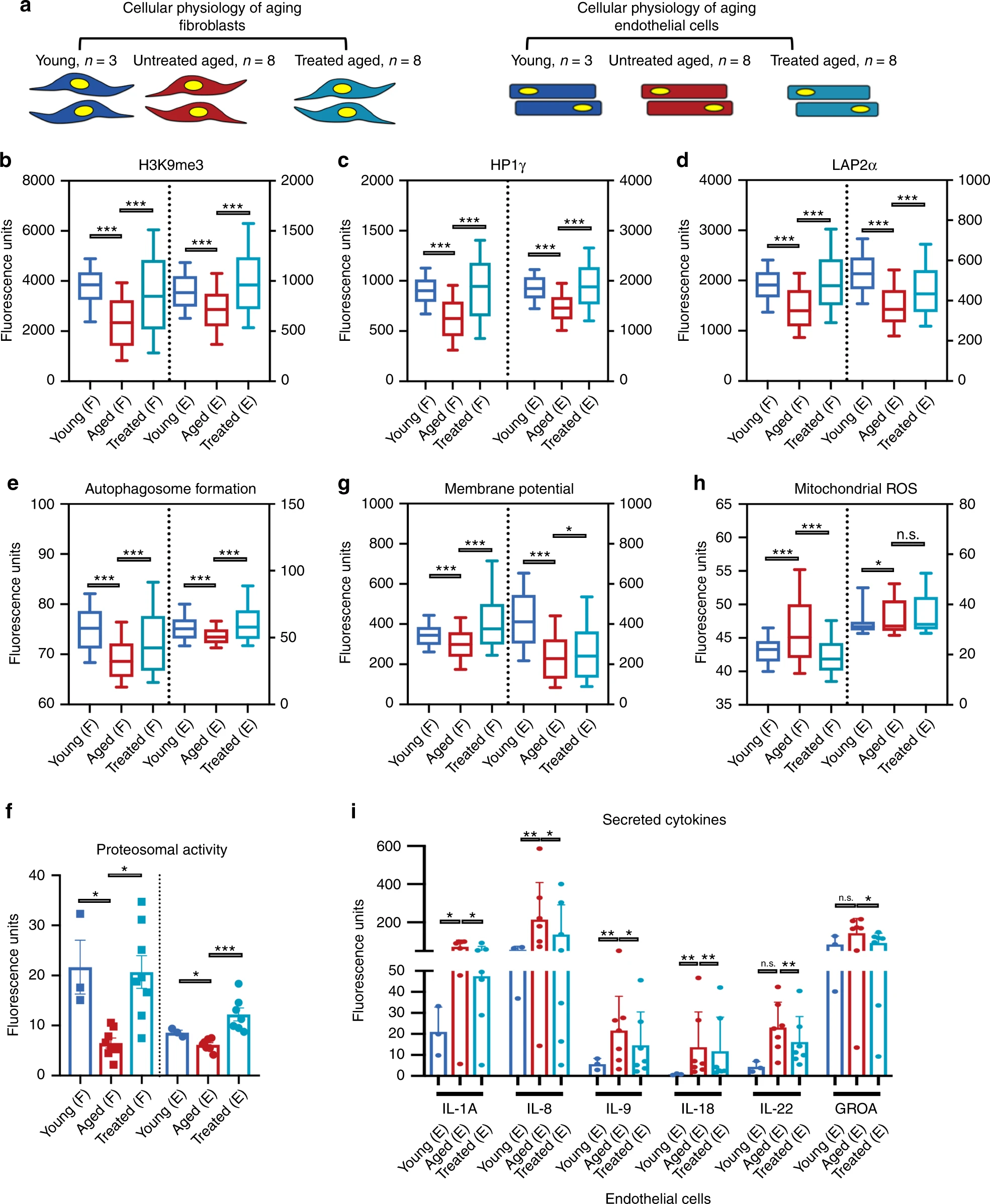 Bild Nr. 2Alle Analysen wurden getrennt in jeder einzelnen Zelllinie ( 2a ) durchgeführt: 19 Linien von Fibroblasten (3 - jung, 8 - älter und 8 - älter nach Reprogrammierung) und 17 Linien von Endothelzellen (3 - jung, 7 - älter und 7 - ältere Menschen nach Neuprogrammierung). Die statistische Analyse wurde durch Zufallsstichprobe von 100 Zellen pro Probe durchgeführt.Um die bisherigen Ergebnisse zur Epigenetik zu erweitern, wurden zusätzliche quantitative Messungen unter Verwendung der Immunfluoreszenz (IF) der epigenetischen repressiven Markierung H3K9me3, des Heterochromatin-assoziierten Proteins HP1γ und des Proteins LAP2α, die das Kernlaminin * ( 2b - 2d ) tragen, durchgeführt.
Bild Nr. 2Alle Analysen wurden getrennt in jeder einzelnen Zelllinie ( 2a ) durchgeführt: 19 Linien von Fibroblasten (3 - jung, 8 - älter und 8 - älter nach Reprogrammierung) und 17 Linien von Endothelzellen (3 - jung, 7 - älter und 7 - ältere Menschen nach Neuprogrammierung). Die statistische Analyse wurde durch Zufallsstichprobe von 100 Zellen pro Probe durchgeführt.Um die bisherigen Ergebnisse zur Epigenetik zu erweitern, wurden zusätzliche quantitative Messungen unter Verwendung der Immunfluoreszenz (IF) der epigenetischen repressiven Markierung H3K9me3, des Heterochromatin-assoziierten Proteins HP1γ und des Proteins LAP2α, die das Kernlaminin * ( 2b - 2d ) tragen, durchgeführt.Nuclear Lamin * - ein fibrilläres starres Netzwerk unter der Kernmembran, das an der Organisation von Chromatin beteiligt ist.
Wie bereits in früheren Studien berichtet, wurde bei reifen Fibroblasten und Endothelzellen bei allen drei Markern im Vergleich zu jungen Zellen eine Abnahme des Kernsignals beobachtet. Die Neuprogrammierung älterer Zellen hat bei beiden Zelltypen zu einem Anstieg dieser Marker geführt.Als nächstes wurde die proteolytische Aktivität (Proteinhydrolyse) von Zellen durch Messen der Bildung von Autophagosomen untersucht, und die chemotrypsinähnliche Proteasomaktivität wurde ebenfalls untersucht. Die Neuprogrammierung erhöhte nicht nur beide Aktivitätsarten auf das Niveau junger Zellen, sondern übertraf es auch ( 2e und 2f ). Dies legt nahe, dass die frühen Stadien der Reprogrammierung zur aktiven Clearance abgebauter Biomoleküle beitragen.Eines der auffälligsten Anzeichen für eine Zellalterung ist eine Abnahme der mitochondrialen Aktivität, die Akkumulation reaktiver Sauerstoffspezies (ROS) und eine Fehlregulation der Nährstoffempfindlichkeit. Daher ist es möglich, den Effekt der Reprogrammierung auf alternde Zellen zu überprüfen, indem das Membranpotential von Mitochondrien, ROS-Mitochondrien und Proteinspiegeln von Sirtuin1 (SIRT1) gemessen wird.Temporäre Reprogrammierung erhöhte das Membranpotential der Mitochondrien in beiden Zelltypen (2 g ), verringerte die mitochondriale ROS ( 2 h) und erhöhte die SIRT1-Proteinspiegel in Fibroblasten, was in jungen Zellen beobachtet wird.Die Bildgebung von Zellen durch Färben von Beta-Galactosidase im Zusammenhang mit dem Altern zeigte eine signifikante Abnahme der Anzahl alternder Zellen in Endothelzellen, jedoch nicht in Fibroblasten. Dies ging einher mit einer Abnahme der Menge an sekretorischen phänotypischen Zytokinen, die mit proinflammatorischem Altern assoziiert sind, und wiederum in Endothelzellen, jedoch nicht in Fibroblasten ( 2i ).Es wurde auch gefunden, dass in keinem der Zelltypen die Telomer * -Länge nach der Neuprogrammierung eine signifikante Verlängerung zeigt. Dies kann darauf hinweisen, dass sich die Zellen nicht in einen Stammzellstil differenzieren, wenn die Telomerase * -Aktivität reaktiviert wird.* — .
* — , 3'- .
Es wurde auch gefunden, dass die Auswirkungen der Reprogrammierung in Zellen auch nach 4 und 6 Tagen nach Beendigung dieses Prozesses bestehen blieben. Unter dem Gesichtspunkt der Geschwindigkeit der Manifestation von Effekten aus der Neuprogrammierung wurden sie bereits 2 Tage nach Beginn dieses Prozesses beobachtet.Insgesamt legen diese Daten nahe, dass die vorübergehende Expression von OSKMLN eine schnelle, kontinuierliche Verbesserung und Veränderung des Zellalters in menschlichen Körperzellen auf Transkriptom-, epigenetischer und zellulärer Ebene bewirken kann. Darüber hinaus tritt diese Verjüngung in den frühen Stadien der Neuprogrammierung auf, aufgrund derer diese Technik keine Zeit hat, die Identität der Zellen zu beeinflussen.Die Wissenschaftler beschlossen dann herauszufinden, ob die vorübergehende Expression von OSKMNL auch die mit dem Altern verbundenen entzündlichen Phänotypen umkehren kann. Nachdem vorläufige Beweise für diese Veränderung der Endothelzellen erhalten wurden ( 2j ), wurde die Analyse durch Hinzufügen von Arthrose erweitert, einer Krankheit, die stark mit dem Altern verbunden ist und durch einen ausgeprägten Entzündungsprozess gekennzeichnet ist, der Chondrozyten in den Gelenken betrifft.Es wurden Proben entnommen - Chondrozyten aus dem Knorpel von sechs Patienten im Alter von 60 bis 70 Jahren, die sich aufgrund einer Arthrose im Spätstadium einer vollständigen Gelenkersatzoperation unterzogen hatten. Ferner wurden diese Proben neu programmiert und die Ergebnisse mit den Daten von Chondrozyten von drei jungen Menschen verglichen ( 3a ). Bild Nr. 3Die temporäre Expression von OSKMLN wurde 2 oder 3 Tage lang durchgeführt, und die Analyse wurde 2 Tage nach Unterbrechung der Reprogrammierung durchgeführt, obwohl die Patienten bei längerer Behandlung eine nachhaltigere Wirkung hatten.Die Verwendung von OSKMLN zeigte jedoch eine signifikante Abnahme der intrazellulären mRNA-Spiegel von RANKL (Zytokin der Familie der Tumornekrosefaktoren) und iNOS2 sowie der Spiegel der von Zellen sezernierten Entzündungsfaktoren ( 3b - 3d ).Zusätzlich wurden eine Zunahme der Zellproliferation ( 3e ), eine Zunahme der ATP-Produktion ( 3f ) und eine Abnahme des Oxidationsprozesses ( 3g und 3h ) beobachtet .Die Überprüfung der Zellidentität zeigte, dass der Reprogrammierungsprozess diese nicht verletzte: Es gab keine Auswirkung auf das Niveau der SOX9-Expression, und das Expressionsniveau von COL2A1 stieg signifikant an (qRT-PCR auf 3i und 3j ).Aus den obigen Ergebnissen folgt, dass die vorübergehende Expression von OSKMLN zu einer teilweisen Umkehrung der Genexpression und der Zellphysiologie in älteren Chondrozyten mit Arthrose in einen jüngeren Zustand beitragen kann. Daher kann die untersuchte Technik auch als eine der Methoden zur Behandlung von Arthrose bei älteren Menschen verwendet werden.Ein weiteres wichtiges Zeichen des Alterns ist der Verlust der Stammzellfunktion und der Verlust der Regenerationsfähigkeit. Um die Auswirkung der Neuprogrammierung auf diese Faktoren zu testen, verwendeten die Wissenschaftler Stammzellen der Skelettmuskulatur von Mäusen (MuSC).MuSCs wurden 2 Tage lang in Ruhe einer Neuprogrammierung ausgesetzt. Personen im Alter von 3 Monaten und 20 bis 24 Monaten ( 4a ) dienten als Probenspender .
Bild Nr. 3Die temporäre Expression von OSKMLN wurde 2 oder 3 Tage lang durchgeführt, und die Analyse wurde 2 Tage nach Unterbrechung der Reprogrammierung durchgeführt, obwohl die Patienten bei längerer Behandlung eine nachhaltigere Wirkung hatten.Die Verwendung von OSKMLN zeigte jedoch eine signifikante Abnahme der intrazellulären mRNA-Spiegel von RANKL (Zytokin der Familie der Tumornekrosefaktoren) und iNOS2 sowie der Spiegel der von Zellen sezernierten Entzündungsfaktoren ( 3b - 3d ).Zusätzlich wurden eine Zunahme der Zellproliferation ( 3e ), eine Zunahme der ATP-Produktion ( 3f ) und eine Abnahme des Oxidationsprozesses ( 3g und 3h ) beobachtet .Die Überprüfung der Zellidentität zeigte, dass der Reprogrammierungsprozess diese nicht verletzte: Es gab keine Auswirkung auf das Niveau der SOX9-Expression, und das Expressionsniveau von COL2A1 stieg signifikant an (qRT-PCR auf 3i und 3j ).Aus den obigen Ergebnissen folgt, dass die vorübergehende Expression von OSKMLN zu einer teilweisen Umkehrung der Genexpression und der Zellphysiologie in älteren Chondrozyten mit Arthrose in einen jüngeren Zustand beitragen kann. Daher kann die untersuchte Technik auch als eine der Methoden zur Behandlung von Arthrose bei älteren Menschen verwendet werden.Ein weiteres wichtiges Zeichen des Alterns ist der Verlust der Stammzellfunktion und der Verlust der Regenerationsfähigkeit. Um die Auswirkung der Neuprogrammierung auf diese Faktoren zu testen, verwendeten die Wissenschaftler Stammzellen der Skelettmuskulatur von Mäusen (MuSC).MuSCs wurden 2 Tage lang in Ruhe einer Neuprogrammierung ausgesetzt. Personen im Alter von 3 Monaten und 20 bis 24 Monaten ( 4a ) dienten als Probenspender .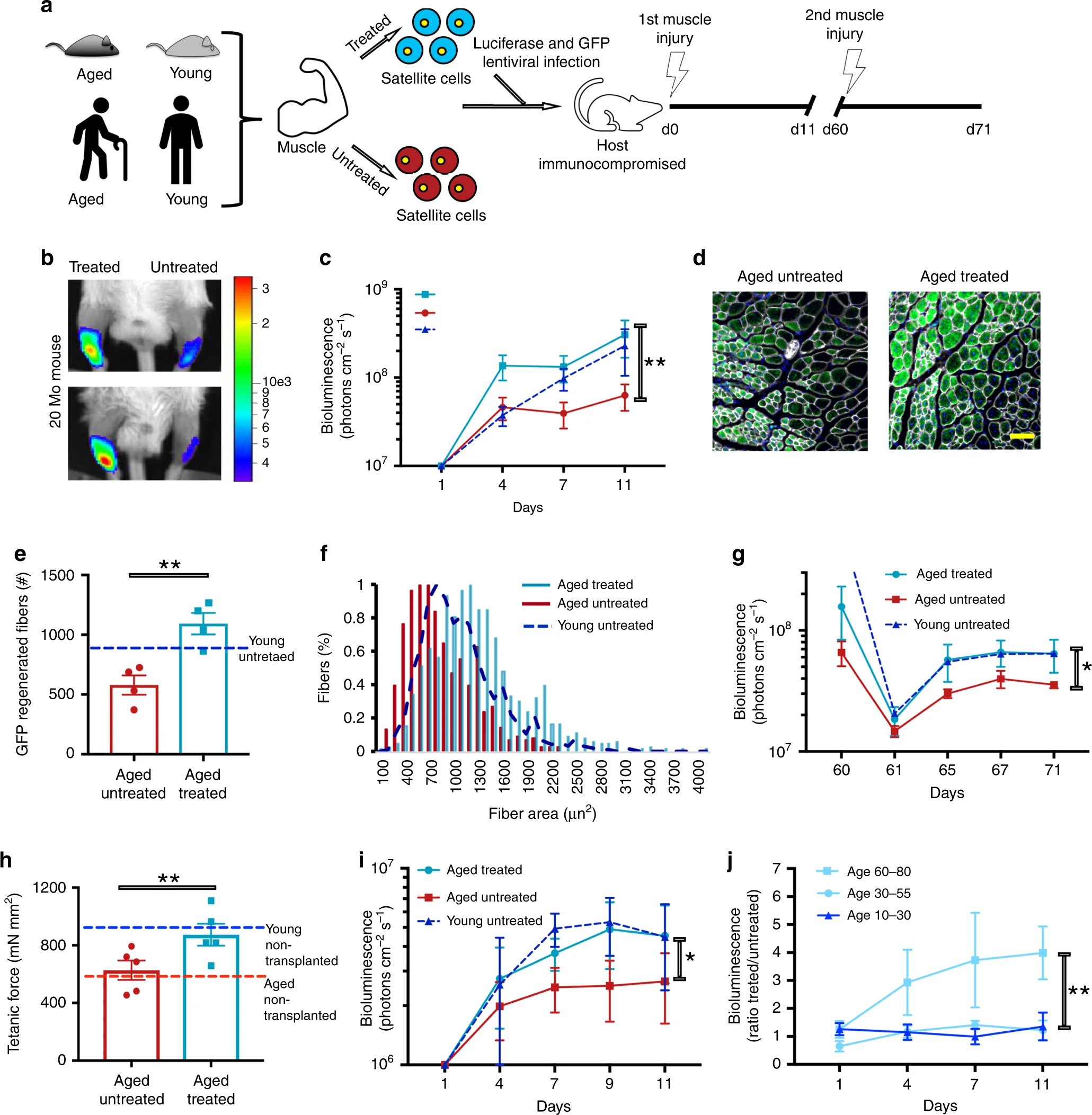 Bild Nr. 4 DieVerarbeitung von altem MuSC verringerte sowohl die Zeit der ersten Teilung als auch die schnellere Kinetik der Aktivierung junger MuSC-Zellen als auch die mitochondriale Masse. Darüber hinaus stellte die Neuprogrammierung teilweise die verringerte Fähigkeit einzelner MuSCs wieder her, Kolonien zu bilden.Als nächstes wurde ein Test der Funktionalität und Wirksamkeit von MuSC hinsichtlich der Regeneration von neuem Gewebe durchgeführt. Zu diesem Zweck wurde die Transduktion von jungen, älteren oder vorübergehend umprogrammierten MuSC-Zellen unter Verwendung von Lentivirus-exprimierender Luciferase und GFP durchgeführt, die dann in beschädigte Muskeln der vorderen Tibia von immungeschwächten Mäusen transplantiert wurden.Die Biolumineszenz-Bildgebung zeigte zunächst, dass die Muskeln, in die die umprogrammierten MuSCs eingebracht wurden, das höchste Signal zeigten (Tag 4; 4b und 4c ). Am 11. Tag ähnelten diese Muskeln jedoch den Muskeln, in denen junge MuSCs hinzugefügt wurden. Die Muskeln, in denen die alternden MuSC-Zellen ohne Neuprogrammierung hinzugefügt wurden, zeigten jedoch die schwächsten Signale ( 4b und 4c))Die Immunfluoreszenzanalyse zeigte, dass Zellen mit Reprogrammierung Gewebe mit mehr Myofibrillen versorgten als Zellen ohne Behandlung ( 4d und 4e ). 60 Tage nach der ersten Analyse wurde eine weitere durchgeführt, die die gleichen Ergebnisse zeigte ( 4 g ). Dies zeigt direkt eine Verbesserung der Regenerationsfähigkeit von Geweben nach Exposition gegenüber Zellen an, die einer Neuprogrammierung unterzogen wurden.In der nächsten Phase der Studie wurde besonderes Augenmerk auf altersbedingte atrophische degenerative Muskelveränderungen gelegt. Die Wissenschaftler beschlossen zu prüfen, ob ihre Technik die Muskelkraft älterer Mäuse auf das Niveau junger Mäuse zurückführen kann.Zunächst wurde die Tetanstärke * in den Muskeln von Mäusen im Alter von 4 und 27 Monaten festgestellt .
Bild Nr. 4 DieVerarbeitung von altem MuSC verringerte sowohl die Zeit der ersten Teilung als auch die schnellere Kinetik der Aktivierung junger MuSC-Zellen als auch die mitochondriale Masse. Darüber hinaus stellte die Neuprogrammierung teilweise die verringerte Fähigkeit einzelner MuSCs wieder her, Kolonien zu bilden.Als nächstes wurde ein Test der Funktionalität und Wirksamkeit von MuSC hinsichtlich der Regeneration von neuem Gewebe durchgeführt. Zu diesem Zweck wurde die Transduktion von jungen, älteren oder vorübergehend umprogrammierten MuSC-Zellen unter Verwendung von Lentivirus-exprimierender Luciferase und GFP durchgeführt, die dann in beschädigte Muskeln der vorderen Tibia von immungeschwächten Mäusen transplantiert wurden.Die Biolumineszenz-Bildgebung zeigte zunächst, dass die Muskeln, in die die umprogrammierten MuSCs eingebracht wurden, das höchste Signal zeigten (Tag 4; 4b und 4c ). Am 11. Tag ähnelten diese Muskeln jedoch den Muskeln, in denen junge MuSCs hinzugefügt wurden. Die Muskeln, in denen die alternden MuSC-Zellen ohne Neuprogrammierung hinzugefügt wurden, zeigten jedoch die schwächsten Signale ( 4b und 4c))Die Immunfluoreszenzanalyse zeigte, dass Zellen mit Reprogrammierung Gewebe mit mehr Myofibrillen versorgten als Zellen ohne Behandlung ( 4d und 4e ). 60 Tage nach der ersten Analyse wurde eine weitere durchgeführt, die die gleichen Ergebnisse zeigte ( 4 g ). Dies zeigt direkt eine Verbesserung der Regenerationsfähigkeit von Geweben nach Exposition gegenüber Zellen an, die einer Neuprogrammierung unterzogen wurden.In der nächsten Phase der Studie wurde besonderes Augenmerk auf altersbedingte atrophische degenerative Muskelveränderungen gelegt. Die Wissenschaftler beschlossen zu prüfen, ob ihre Technik die Muskelkraft älterer Mäuse auf das Niveau junger Mäuse zurückführen kann.Zunächst wurde die Tetanstärke * in den Muskeln von Mäusen im Alter von 4 und 27 Monaten festgestellt .Tetanus * - ein Zustand längerer Muskelkontraktion.
Wie erwartet war diese Stärke bei älteren Mäusen signifikant geringer als bei jungen Mäusen, was auf einen Altersfaktor ( 4 Stunden ) hinweist .Dann wurden MuSC-Zellen aus Mäusen im Alter von 20 bis 24 Monaten isoliert, die später einem Umprogrammierungsprozess unterzogen wurden, und dann in einen mit Cardiotoxin geschädigten Muskel von Mäusen im Alter von 20 Monaten transplantiert. Nach 30 Tagen wurden die Tetanstärkemessungen wiederholt.Die Muskeln, in die die Zellen ohne Neuprogrammierung transplantiert wurden, zeigten die gleichen Ergebnisse wie die normalen Muskeln älterer Mäuse ohne Intervention. Die Muskeln, in denen die Zellen mit Neuprogrammierung platziert wurden, zeigten jedoch Tetankräfte, die mit den Muskeln junger Mäuse vergleichbar waren ( 4 Stunden ).Daraus folgt, dass eine vorübergehende Neuprogrammierung in Kombination mit einer MuSC-basierten Therapie die physiologische Funktion alternder Muskeln auf die Funktionen junger Muskeln zurückführen kann.Die Durchführung eines ähnlichen Verfahrens mit Muskeln und menschlichen Zellen zeigte ähnlich positive Ergebnisse ( 4i und 4j ).Um die Nuancen der Studie genauer kennenzulernen, empfehle ich Ihnen, den Bericht von Wissenschaftlern und zusätzliche Materialien zu lesen.Epilog
In der heute untersuchten Studie konnten Wissenschaftler eine vorübergehende Neuprogrammierung von Zellen nachweisen, die die Zeichen der Zellalterung bekämpfen und die zelluläre Identität nicht beeinflussen kann.Zellen älterer Menschen, die einer Neuprogrammierung unterzogen wurden, zeigen nach einigen Tagen die Eigenschaften junger Zellen. In diesem Fall bleibt die Wirkung sechs Tage nach Beendigung der Behandlung bestehen.Diese Technik ist nicht nur im Hinblick auf die allgemeine Verjüngung von Zellen und Geweben wichtig, sondern insbesondere auch im Hinblick auf die Bekämpfung der Auswirkungen altersbedingter Krankheiten wie Arthrose.In Zukunft wollen Wissenschaftler ihre Methodik verbessern. Erstens ist es, wie die Forscher selbst sagen, notwendig, viele Tests im Labor durchzuführen und die Sicherheit der Methode auf Zellebene vollständig zu überprüfen. Danach kann die Verwendung auf Gewebeebene beginnen.Ist die Menschheit in Bezug auf Moral, Ethik und Psychologie bereit für die ewige Jugend? Die Frage ist komplex, hat aber viele Antworten. Der Zweck dieser Studie ist jedoch nicht die Suche nach Unsterblichkeit, sondern die Suche nach neuen wirksamen Methoden zur Bekämpfung verschiedener Krankheiten, die im Zusammenhang mit der unvermeidlichen Alterung des Körpers auftreten. Das Alter ist nicht so schlimm wie die damit verbundenen Krankheiten. Das Gleiche gilt für jedes Alter. Für welche Freude gibt es in der mythischen ewigen Jugend, wenn ein Mensch für all diese Ewigkeit mit Schmerzen zu kämpfen hat?Freitag off-top:
, , , , . ( / Anastatica hierochuntica).
Vielen Dank für Ihre Aufmerksamkeit, bleiben Sie neugierig und wünschen Sie allen ein schönes Wochenende! :) :)Ein bisschen Werbung :)
Vielen Dank für Ihren Aufenthalt bei uns. Gefällt dir unser Artikel? Möchten Sie weitere interessante Materialien sehen? Unterstützen Sie uns, indem Sie eine Bestellung aufgeben oder Ihren Freunden Cloud-basiertes VPS für Entwickler ab 4,99 US-Dollar empfehlen , ein einzigartiges Analogon von Einstiegsservern, das von uns für Sie erfunden wurde: Die ganze Wahrheit über VPS (KVM) E5-2697 v3 (6 Kerne) 10 GB DDR4 480 GB SSD 1 Gbit / s ab 19 $ oder wie teilt man den Server? (Optionen sind mit RAID1 und RAID10, bis zu 24 Kernen und bis zu 40 GB DDR4 verfügbar).Dell R730xd 2-mal günstiger im Equinix Tier IV-Rechenzentrum in Amsterdam? Nur wir haben 2 x Intel TetraDeca-Core Xeon 2x E5-2697v3 2,6 GHz 14C 64 GB DDR4 4 x 960 GB SSD 1 Gbit / s 100 TV von 199 US-Dollar in den Niederlanden!Dell R420 - 2x E5-2430 2,2 GHz 6C 128 GB DDR3 2x960 GB SSD 1 Gbit / s 100 TB - ab 99 US-Dollar! Lesen Sie, wie Sie eine Infrastruktur aufbauen Klasse C mit Dell R730xd E5-2650 v4-Servern für 9.000 Euro für einen Cent?